Neue Mechanismen der Tumormetastasierung
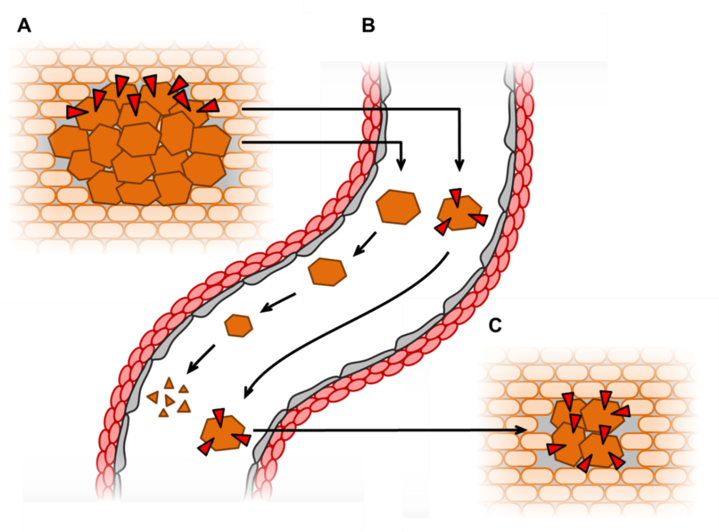
Abbildung 1: Einfluss von CEACAM1 auf die Anoikis von Tumorzellen
A) Im Zellverband befindliche Tumorzellen (prominent dargestellt) erhalten durch ihre Umgebung Überlebenssignale. B) Nachdem sich die Tumorzellen aus dem Zellverband gelöst haben, entfallen diese Überlebenssignale. Dies führt im Blutstrom/Lymphe zum Absterben (Anoikis) der Tumorzellen, die kein CEACAM1 exprimieren (links). Tumorzellen, die CEACAM1 exprimieren (rote Dreiecke, rechts), können im Blutstrom überleben und anschließend C) an anderer Stelle im Körper Metastasen bilden.
Team
Das interdisziplinäre Forschungsteam um Herrn Dr. Florian Kleefeldt setzt sich aus erfahrenen BiologInnen, technischen AssistentInnen und DoktorandInnen zusammen.
Motivation
Tumorerkrankungen stellen eine der Haupttodesursachen weltweit dar. Ein großer Teil der Patienten verstirbt hierbei nicht am Primärtumor selbst, sondern an dessen Metastasen, Absiedelungen von Tumorzellen, die über das Blut- und/oder Lymphsystem in andere Organe eingewandert sind. Eine solche Wanderung ehemals residenter Zellen erfordert aber die Überwindung verschiedener Sicherungsmechanismen. So erhalten normale, nicht entartete Zellen durch ihre Verankerung im Zellverband Überlebenssignale. Lösen sich diese Zellen aus ihrem Verband entfallen diese Signale und die Zellen gehen durch Anoikis, einer speziellen Form der Apoptose, zugrunde. Metastasierende Tumorzellen können sich diesem Mechanismus entziehen.
Klinische Untersuchungen unterschiedlicher Tumorentitäten (u.a. Haut-, Dickdarm-, Lungen- und Blasenkrebs) zeigen, dass das Protein CEACAM1 (Carcinoembryonic antigen-related cell adhesion molecule 1) in metastasierenden Tumoren wesentlich stärker als in nicht-metastasierenden, lokal begrenzen Tumoren exprimiert wird. Zudem konnten wir in Vorarbeiten bereits in vitro zeigen, dass CEACAM1 maßgeblich die Anoikis in Lungentumorzellen vermindert. Dies stellt einen neuartigen Mechanismus dar, der die Metastasierung von Tumorzellen ermöglicht.
Welche Ziele verfolgt das Projekt?
Ziel dieses Projektes ist es daher, die Signalwege aufzudecken, über die CEACAM1 in Tumorzelllinien verschiedener Entitäten Anoikis vermindert. Zudem werden wir überprüfen, ob sich CEACAM1 als therapeutische Zielstruktur zur Prävention und Behandlung metastasierender Tumoren eignet.
Ansatz des Forschungsprojektes
Für dieses Projekt verfolgen wir einen „bench-to-bedside“ Ansatz. Zunächst werden wir in der Zellkultur überprüfen, ob sich unsere Vorarbeiten auf weitere Tumorentitäten übertragen lassen. An den verschiedenen Tumorzelllinien sollen auch die Signalwege aufgeklärt werden, über die CEACAM1 die Anoikis vermindert und damit die Metastasierung von Tumorzellen ermöglicht. Diese in vitro gewonnenen Erkenntnisse sollen anschließend im Tiermodell evaluiert werden. Darüber hinaus werden wir im Tiermodell auch überprüfen, ob sich CEACAM1 als therapeutische Zielstruktur eignet, um die Metastasierung von Tumorzellen zu verhindern. Dazu verfügen wir über CEACAM1-Inhibitoren, welche später ebenfalls im Patienten Anwendung finden könnten. Eine Finanzierung dieses Projektes über die Stiftung „Forschung hilft!“ könnte somit einen wichtigen Grundstein für die Entwicklung eines neuen Therapiekonzeptes in der Behandlung metastasierender Tumoren legen.
Welche Krebserkrankung soll behandelt werden?
Basierend auf den klinischen Daten scheint es sich um einen generellen Mechanismus zu handeln, über den CEACAM1 die Metastasierung von Tumorzellen begünstigen könnte. Daher handelt es sich um einen neuartigen Ansatz, bei dem unabhängig von der Tumorentität CEACAM1 als therapeutische Zielstruktur genutzt werden könnte.
Warum soll das Forschungsprojekt unterstützt werden?
Bisher stehen für viele Krebserkrankungen im metastasierten Stadium keine effizienten Therapieoptionen zur Verfügung. Im Rahmen dieses Projektes werden wir einen neuartigen Therapieansatz überprüfen. Wir hoffen hierüber einen Beitrag zur Verbesserung der Therapie von Patienten mit metastasierenden Tumorerkranken leisten zu können.
