Künstliche Intelligenz zur Erkennung von Rezidiven nach Entfernung von Dickdarmkrebs und Vorstufen

Abbildung 1: Teamfoto der Arbeitsgruppe.
TEAM
Die Arbeitsgruppe ist ein interprofessionelles Team unter der Leitung von Univ.-Prof. Dr. med. Alexander Hann am Universitätsklinikum Würzburg. Es vereint Mitglieder aus der Medizin mit langjähriger Expertise auf dem Gebiet der künstlichen Intelligenz (KI) mit Mitgliedern aus dem Bereichen Ingenieurwesen und Informatik. Hinzu kommen Medizinstudierende und Informatikstudierende, die ihre Bachelor-, Master- oder Doktorarbeit in der Arbeitsgruppe absolvieren (Abbildung 1).

Abbildung 2: Jana Theile, wissenschaftliche Mitarbeiterin und Ärztin, als Bindeglied zwischen dem technischen und dem klinischen Team in der Projektentwicklung (links). Dr. Ioannis Kafetzis, Leiter des KI-Teams mit dem Schwerpunkt auf Entwicklung, klinische Implementierung und Evaluation von KI-Systemen in der Routineversorgung (rechts).
Motivation und Innovation
Durch die Beteiligung von Ärztinnen und Ärzten in der Arbeitsgruppe werden Probleme aus der täglichen Patientenversorgung im Bereich Krebsvorsorge und Krebsbehandlung direkt aufgegriffen. In direktem Kontakt mit Teammitgliedern aus den Bereichen Informatik, Mathematik und Ingenieurswissenschaften werden dann Lösungen in der Gruppe erarbeitet (Abbildung 3). Das Ziel bleibt dabei immer durch die Verbesserung von klinischen Arbeitsabläufen den Patientinnen und Patienten in der Klinik direkt helfen zu können. Eine wesentliche Rolle in diesem Vorhaben spielen Jana Theile als wissenschaftliche Mitarbeiterin und Ärztin und Dr. Ioannis Kafetzis als Mathematiker und KI-Entwickler (Abbildung 2). Jana Theile promoviert im Bereich Künstliche Intelligenz in der Endoskopie und ist als Bindeglied zwischen dem technischen und dem klinischen Team direkt an der Projektentwicklung beteiligt. Durch ihre medizinische Ausbildung und ihre Arbeit an der Schnittstelle beider Bereiche bringt sie sowohl klinisches Wissen als auch technisches Verständnis in das Projekt ein. Dr. Ioannis Kafetzis leitet das KI-Team mit dem Schwerpunkt auf die Entwicklung, klinische Implementierung und Evaluation von KI-Systemen in der Routineversorgung. Ziel seiner Arbeit ist es, robuste, zuverlässige und in der Praxis wirksame Systeme zu entwickeln.

Abbildung 3: Interdisziplinäre Diskussion von medizinischen Problemstellungen (links), Interdisziplinärer Aufbau und Durchführung der Experimente mit unserem Endoskopieturm für Forschungsprojekte (mitte), Arbeit am Prototyp für einen Virtual Reality (VR) Endoskopie Simulator (rechts).
Welche Ziele verfolgt das Projekt?
Die Darmspiegelung (Koloskopie) kann sowohl zur Vorsorge, als auch zur Behandlung von Darmkrebs eingesetzt werden. Dabei werden Darmkrebs und frühe Krebsvorstufen direkt während der Untersuchung entfernt (Resektion). Nach der Entfernung bleibt eine Narbe im Darm zurück (Abbildung 4). Im Bereich dieser Narbe kann es jedoch zu einem Wiederauftreten der entfernten Veränderungen kommen. In diesem Fall spricht man von einem Rezidiv. Bei Kontrollen werden diese Narben daher gezielt aufgesucht und sorgfältig auf das Vorhandensein von Rezidiven untersucht. Die Rezidiverkennung, vor allem im frühen Stadium, ist jedoch manchmal sehr schwierig, weshalb diese übersehen werden können.
Mit unserem Projekt wollen wir eine Künstliche Intelligenz (KI) entwickeln, welche Untersuchende dabei unterstützt Narben, nach der Entfernung von Krebs und Vorstufen, schneller und zuverlässiger aufzufinden. Sobald das System eine Narbe entdeckt soll es den Untersuchenden benachrichtigen, sodass die Stelle noch einmal mit spezialisierter Bildgebung untersucht werden kann. So soll ein Wiederauftreten der Veränderungen rechtzeitig und ein Fortschreiten so früh wie möglich verhindert werden.
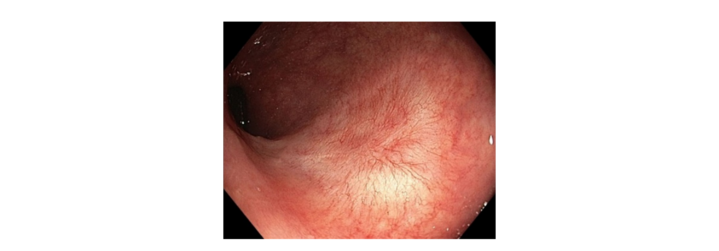
Abbildung 4: Resektionsnarbe im endoskopischen Bild während einer Darmspiegelung
Ansatz des Forschungsprojektes
Darmkrebs ist bei Frauen die zweithäufigste und bei Männern die dritthäufigste Krebserkrankung. Außerdem stellt er die dritthäufigste krebsbedingte Todesursache in Deutschland dar. [1,2] Eine Früherkennung von Darmkrebsvorstufen senkt deutlich die Erkrankungszahl und die damit verbundenen Todesfälle. Die Darmspiegelung (Koloskopie) ist die zuverlässigste Methode zur Früherkennung, Überwachung und Behandlung von Veränderungen im Dickdarm, mit deren Hilfe krankhaftes Gewebe besonders sicher und verlässlich erkannt werden kann [3]. Kleine Wucherungen der Darmschleimhaut (Polypen) gelten als mögliche Krebsvorstufen, weshalb bereits eine frühzeitige und komplette Entfernung (Resektion) empfohlen wird [3]. Für kleinere Polypen bis 3mm wird eine Resektion mittels Biopsiezange empfohlen, für größere wird eine Schlingenresektion oder eine endoskopische Mukosaresektion (EMR) als Standardverfahren genutzt [3–5]. Nach der Entfernung heilt die betroffene Stelle innerhalb weniger Tage bis Wochen ab und hinterlässt eine Narbe im Darm. Eine unvollständige Entfernung von Schleimhautveränderungen stellt ein deutliches Risiko für ein Wiederauftreten (Rezidiv) von Darmkrebs und dessen Vorstufen an derselben Stelle dar.
Werden Krebsvorstufen entfernt wird bei den Patienten je nach Befund eine Kontrolluntersuchung in einem festgelegten Zeitraum, teilweise bereits nach 6 Monaten, durchgeführt. Bei dieser Kontrolle wird die Narbe gezielt aufgesucht und genau untersucht, um sicherzustellen, dass kein erneutes Wachstum stattgefunden hat [6]. Der Einsatz von speziellen Bildtechniken kann die Erkennungsrate von verdächtigen Veränderungen während der Narbenbegutachtung dabei deutlich verbessern.
Bei bestimmten Polypenarten kommt es in bis zu 20% der Fälle innerhalb eines Jahres zur Ausbildung eines Rezidivs [7]. Wird ein Rezidiv festgestellt, wird das erneut gewachsene Gewebe in der Regel direkt während der Kontrolluntersuchung erneut entfernt [5].
In einigen Fällen lassen sich die Resektionsstellen und Narben im Verdauungstrakt jedoch nur schwer oder gar nicht mehr auffinden. Selbst wenn Narben identifiziert werden, werden nicht immer vorhandene Rezidive erkannt. In bis zu 13% der Rezidive werden diese nicht durch den Untersuchenden, sondern erst durch eine feingewebliche (histologische) Untersuchung erkannt [10,11]. Dabei handelt es sich um äußerlich unauffällige Narben, welche jedoch trotzdem restliche Zellen der ursprünglichen Veränderung enthalten.
Künstliche Intelligenz (KI) hat im Bereich der Vorsorge große Erfolge erzielt und wird bereits in der täglichen Praxis in der Medizin und auch während der Endoskopie eingesetzt, beispielsweise zur automatisierten Geschwindigkeitsmessung während der Untersuchung, Größenmessung von Polypen und zur Polypendetektion [12–14]. Es gibt im Bereich der Endoskopie jedoch noch keine Modelle zum Erkennen von Narben im Verdauungstrakt.
Die Arbeitsgruppe hat bereits eigene KIs entwickelt und in multizentrischen Studien evaluiert [13,15–18]. Um diesem Problem des Wiederauffindens von Narben und dem Identifizieren von Rezidiven zu begegnen, wollen wir ein KI-Modell entwickeln, welches in endoskopischem Bildmaterial Resektionsnarben erkennen kann. Daraus ergibt sich die Möglichkeit zur Entwicklung eines Systems, welches auf diese Narben aufmerksam machen kann. Ebenso können Narben anhand ihrer Erscheinung bewertet und eingeordnet werden. Eine Integration eines solchen Assistenzsystems in den klinischen Alltag kann in Zukunft die klinische Entscheidungsfähigkeit von Untersuchenden stärken und unnötige Probenentnahmen reduzieren.
Jährlich werden am Uniklinikum Würzburg ca. 8000 Koloskopien durchgeführt. Wir haben einen Bilddatensatz von 1998 bis 2021, welchen wir rückblickend analysieren können. Zur Entwicklung der KI wird dieser Datensatz und zugehörige Berichte ausgewertet. Zudem werden Ergebnisse feingeweblich (histologisch) gesicherter Probeentnahmen einbezogen. Ein Arzt oder eine Ärztin schaut sich dann alle Bilder der Darmspiegelungen einzeln an und markiert darauf, wo sich Narben befinden, die nach der Entfernung von Krebsvorstufen und Krebs entstanden sind. Mit diesen Informationen wird auf unseren Graphikkartenservern eine KI trainiert. Im nächsten Schritt wird die tatsächliche Leistung und Genauigkeit der KI bewertet.
Die entwickelte KI kann genutzt werden, um aus Bildmaterial von neuen Untersuchungen rückblickend Resektionsnarben zu erkennen. Ein lokales Large Language Modell (LLM) kann dabei parallel die Untersuchungsberichte textbasiert untersuchen und Unstimmigkeiten können durch dieses System, bestehen aus zwei KI-Modellen berichtet werden. Eine Echtzeit Integration in den klinischen Arbeitsablauf parallel zu den Untersuchungen ist im Verlauf ebenfalls möglich. Das System kann das Bildmaterial direkt während der Untersuchung analysieren und bei Erkennung einer Resektionsnarbe den Untersuchenden auf diese aufmerksam macht.
Welche Krebserkrankung soll behandelt werden?
Darmkrebs ist in Deutschland je nach Geschlecht die zweit-/dritthäufigste Krebserkrankung. Durch regelmäßige Vorsorge-Darmspiegelungen können Vorstufen frühzeitig entfernt und so das Risiko, an Darmkrebs zu erkranken, deutlich gesenkt werden. Je zuverlässiger bei Kontrollen Narben und frühe Rezidive erkannt werden, desto besser können Betroffene behandelt und schwere Krankheitsverläufe verhindert werden.
Künstliche Intelligenz kann dabei in zwei wichtigen Bereichen helfen. In der Vorsorge kann sie zur Polypenerkennung genutzt werden und bei Kontrolluntersuchungen zur Erkennung von erneuten Gewebewucherungen in bereits behandelten Stellen.
Warum soll das Forschungsprojekt unterstützt werden?
Durch die Entwicklung einer KI zur Erkennung von Narben und möglichen Rezidiven kann die Nachsorge von Patientinnen und Patienten deutlich verbessert werden. Rezidive können früher erkannt und behandelt werden, bevor sie sich weiterentwickeln. Das verbessert die Heilungschancen und kann im besten Fall lebensrettend sein. Die Ergebnisse dieser Forschung sowie die entwickelte KI werden anschließend veröffentlicht, sodass andere Forschungsgruppen weltweit darauf aufbauen können. Darüber hinaus kann die Technologie direkt von der Medizinprodukteindustrie genutzt werden, um sie in zukünftige Geräte für die Darmspiegelung zu integrieren.
Literaturverzeichnis
- Krebs - Krebsarten [Internet]. [cited 2026 Apr 28]. Available from: https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/krebsarten_node.html
- Krebs - Kurzbeiträge - Altersstandardisierte Krebssterblichkeit ging auch 2020 weiter zurück [Internet]. [cited 2026 Apr 28]. Available from: https://www.krebsdaten.de/Krebs/DE/Content/Publikationen/Kurzbeitraege/Archiv2021/2021_6_Todesursachenstatistik_krebssterblichkeit.html
- Langer T. S3-Leitlinie Kolorektales Karzinom. 2026.
- Kaltenbach T, Anderson JC, Burke CA, Dominitz JA, Gupta S, Lieberman D, et al. Endoscopic Removal of Colorectal Lesions: Recommendations by the US Multi-Society Task Force on Colorectal Cancer. Official journal of the American College of Gastroenterology | ACG. 2020 Mar;115(3):435. doi:10.14309/ajg.0000000000000555
- Ferlitsch M, Hassan C, Bisschops R, Bhandari P, Dinis-Ribeiro M, Risio M, et al. Colorectal polypectomy and endoscopic mucosal resection: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2024. Endoscopy. 2024 Apr 26;56:516–45. doi:10.1055/a-2304-3219
- Hassan C, Antonelli G, Dumonceau JM, Regula J, Bretthauer M, Chaussade S, et al. Post-polypectomy colonoscopy surveillance: European Society of Gastrointestinal Endoscopy (ESGE) Guideline – Update 2020. Endoscopy. 2020 Aug;52(8):687–700. doi:10.1055/a-1185-3109
- Pellise M, Burgess NG, Tutticci N, Hourigan LF, Zanati SA, Brown GJ, et al. Endoscopic mucosal resection for large serrated lesions in comparison with adenomas: a prospective multicentre study of 2000 lesions. Gut. 2017 Apr;66(4):644–53. doi:10.1136/gutjnl-2015-310249
- Desomer L, Tutticci N, Tate DJ, Williams SJ, McLeod D, Bourke MJ. A standardized imaging protocol is accurate in detecting recurrence after EMR. Gastrointestinal Endoscopy. 2017 Mar 1;85(3):518–26. doi:10.1016/j.gie.2016.06.031
- João M, Areia M, Pinto-Pais T, Gomes LC, Saraiva S, Alves S, et al. Can white-light endoscopy or narrow-band imaging avoid biopsy of colorectal endoscopic mucosal resection scars? A multicenter randomized single-blind crossover trial. Endoscopy. 2023 Feb 24;55:601–7. doi:10.1055/a-2018-1612
- Steinbrück I, Ebigbo A, Kuellmer A, Schmidt A, Kouladouros K, Brand M, et al. Cold Versus Hot Snare Endoscopic Resection of Large Nonpedunculated Colorectal Polyps: Randomized Controlled German CHRONICLE Trial. Gastroenterology. 2024 Sep;167(4):764–77. doi:10.1053/j.gastro.2024.05.013 PubMed PMID: 38795735.
- Meulen LWT, Bogie RMM, Siersema PD, Winkens B, Vlug MS, Wolfhagen FHJ, et al. Optical assessment of scars after endoscopic mucosal resection of large colorectal polyps in a multicenter, community hospital setting: is routine biopsy still necessary? Endoscopy. 2025 Jan 28;57(6):620–8. doi:10.1055/a-2498-7114 PubMed PMID: 39653123; PubMed Central PMCID: PMC12119144.
- Lui TKL, Ko MKL, Liu JJ, Xiao X, Leung WK. Artificial intelligence–assisted real-time monitoring of effective withdrawal time during colonoscopy: a novel quality marker of colonoscopy. Gastrointestinal Endoscopy. 2024 Mar 1;99(3):419-427.e6. doi:10.1016/j.gie.2023.10.035
- Sudarevic B, Sodmann P, Kafetzis I, Troya J, Lux TJ, Saßmannshausen Z, et al. Artificial intelligence-based polyp size measurement in gastrointestinal endoscopy using the auxiliary waterjet as a reference. Endoscopy. 2023 Sep;55(9):871–6. doi:10.1055/a-2077-7398
- Lee JY, Jeong J, Song EM, Ha C, Lee HJ, Koo JE, et al. Real-time detection of colon polyps during colonoscopy using deep learning: systematic validation with four independent datasets. Sci Rep. 2020 May 20;10(1):8379. doi:10.1038/s41598-020-65387-1
- Lux TJ, Banck M, Saßmannshausen Z, Troya J, Krenzer A, Fitting D, et al. Pilot study of a new freely available computer-aided polyp detection system in clinical practice. Int J Colorectal Dis. 2022 Jun 1;37(6):1349–54. doi:10.1007/s00384-022-04178-8
- Lux TJ, Saßmannshausen Z, Kafetzis I, Banck M, Krenzer A, Fitting D, et al. Artificial intelligence assisted colorectal lesion detection in private practices a randomized controlled study. npj Digit Med. 2026 Apr 1;9(1):284. doi:10.1038/s41746-026-02576-8
- Lux TJ, Saßmannshausen Z, Kafetzis I, Sodmann P, Herold K, Sudarevic B, et al. Assisted documentation as a new focus for artificial intelligence in endoscopy: the precedent of reliable withdrawal time and image reporting. Endoscopy. 2023 Dec;55(12):1118–23. doi:10.1055/a-2122-1671
- Kafetzis I, Sodmann P, Herghelegiu BE, Pauletti M, Brand M, Schöttker K, et al. A prospective study evaluating an artificial intelligence-based system for withdrawal time measurement. Endoscopy. 2026 Apr;58(4):367–75. doi:10.1055/a-2721-6798
