Ursachen und Therapie von Blutungskomplikationen beim Nebennierenkarzinom unter Mitotane-Therapie

Abbildung 1: Teamfoto der Arbeitsgruppe
TEAM
Die Arbeitsgruppe von Dr. Lukas Weiß untersucht, wie die Interaktion von Thrombozyten mit Immunzellen zu Blutungs- und Thrombosekomplikationen beiträgt. Mit einem jungen und interdisziplinären Team bearbeiten wir diese Fragestellungen in enger Kooperation mit den Medizinischen Kliniken, dem Institut für Experimentelle Biomedizin und dem Deutschen Zentrum für Herzinsuffizienz. In unserer Arbeit zum Nebennierenkarzinom arbeiten wir besonders eng mit dem Team von Prof. Dr. Martin Faßnacht (Lehrstuhl für Endokrinologie und Diabetologie), Prof. Dr. Harald Schulze (Institut für Experimentelle Biomedizin) und Prof. Dr. Christoph Maack (Deutsches Zentrum für Herzinsuffizienz) zusammen.
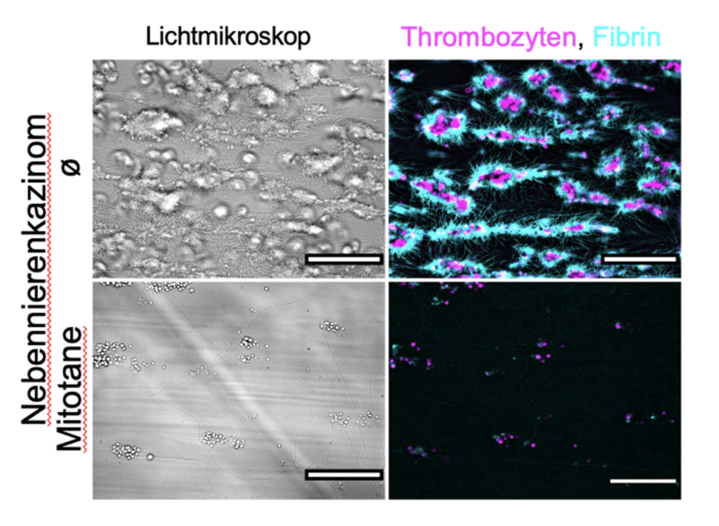
Abbildung 2: In einem Thrombosemodell verwenden wir Blut von Patienten mit Nebnnierenkarzinom vor Mitotane-Therapie (ø) und nach Beginn der Mitotane-Therapie. Wir sehen, dass nach Beginn der Therapie weniger Thrombozyten haften bleiben und die Bildung von Fibrin stark eingeschränkt ist, was für einen Defekt der Gerinnung spricht.
Motivation und Innovation
Das Nebennierenrindenkarzinom ist eine eher seltene, aber sehr aggressive Tumorerkrankung, welche von den hormonproduzierenden Zellen der Nebennierenrinde ausgeht und insbesondere auch bei jüngeren Patienten zwischen dem 20. und 30. Lebensjahr auftritt. Neben Tumorwachstum und Metastasierung kommt es zu einer überschießenden Hormonfreisetzung, was zu Bluthochdruck, Entgleisungen des Zuckerstoffwechsels, Muskelschwäche und vermehrter Körperbehaarung bei Frauen führt. Dies kann für die Patienten zusätzlich sehr belastend sein.
Die Prognose des Nebennierenkarzinoms ist insgesamt eher ungünstig, da die Erkrankung häufig spät diagnostiziert wird und die Anzahl an wirksamen medikamentösen Therapieoptionen limitiert ist. Das einzige weltweit für die Therapie des Nebennierenkarzinoms zugelassene Medikament ist Mitotane. Trotz dieser zentralen Rolle gestaltet sich die Behandlung mit Mitotane oft schwierig, da sie mit erheblichen Nebenwirkungen einher gehen kann. Eine seit Jahrzehnten bekannte Nebenwirkung sind Blutungsereignisse, die für die Betroffenen eine erhebliche Gefährdung (v.a. während einer Operation) darstellen und dazu führen, dass die Tumortherapie unterbrochen werden muss. Der Grund, warum Mitotane-Therapie zu Blutungsereignissen führt, ist bislang nicht bekannt und die zugrundeliegenden Mechanismen sind unverstanden.
In einer Pilotarbeit konnten wir in den letzten Jahren zeigen, dass die Mitotane-Therapie direkt zu einer Verschlechterung der Funktion der Thrombozyten (Blutplättchen) führt (Abbildung 2), welche normalerweise beim gesunden Organismus die Stillung von Blutungen vermitteln. Unsere Daten zeigen, dass die Blutplättchen umso schlechter funktionieren, je höher der Mitotane-Spiegel im Blut ist. Dieser Effekt lässt sich auch in vitro (im Reagenzglas) durch die direkte Zugabe von Mitotane zu den Blutplättchen nachvollziehen. Gemeinsam mit unseren Kollegen vom Deutschen Zentrum für Herzinsuffizienz konnten wir zeigen, dass Mitotane die Funktion der Mitochondrien stört, welche die Zellen normalerweise mit Energie versorgen. Dabei scheint besonders das Protein SOAT1 eine Schlüsselrolle zu spielen, welches von Mitotane gehemmt wird. Basierend auf diesen Vordaten gehen wir davon aus, dass genau hier die Ursache der Blutungskomplikationen liegt.
Unsere Motivation hinter dieser Arbeit ist es, diesen Mechanismus zu verstehen und die Therapie der Patienten mit Nebennierenkarzinom dadurch entscheidend zu verbessern. Unser Projekt ist äußerst innovativ, da wir in einem translationalen Ansatz erstmalig ein seit Jahrzehnten bestehendes klinisches Problem adressieren. Dabei stellen wir einen vollkommen unbekannten mechanistischen Zusammenhang zwischen dem Protein SOAT1, Dysfunktion der Mitochondrien und der Blutungsneigung beim Nebennierenrindenkarzinom in den Fokus.
"Mitotane ist unverzichtbarer Bestandteil der Therapie des Nebennierenrindenkarzinoms, zugleich können Blutungskomplikationen die Behandlung erheblich erschweren. Die Aufklärung dieses klinisch hochrelevanten Problems besitzt daher unmittelbare Bedeutung für die Versorgung unserer Patientinnen und Patienten.“
Univ.-Prof. Dr. Martin Faßnacht, Leiter des Lehrstuhls für Endokrinologie und Diabetologie
Welche Ziele verfolgt das Projekt?
Unser Projekt verfolgt vier konkrete Ziele, um die Behandlung von Patientinnen und Patienten mit Nebennierenrindenkarzinom gezielt zu verbessern.
- Wir wollen untersuchen, wie Mitotane als einzige zugelassene medikamentöse Therapie des Nebennierenrindenkarzinoms über SOAT1 die mitochondriale Funktion und die Aktivität von Thrombozyten beeinflusst.
- Wir möchten klären, ob diese Therapie nur reife Thrombozyten in ihrer Funktion beeinträchtigt, oder auch deren Entstehung aus Vorläuferzellen im Knochenmark stört.
- Wir wollen analysieren, wie sich diese Veränderungen auf Blutstillung und Thrombusbildung auswirken und so zu den Blutungskomplikationen beitragen, die die Behandlung des Nebennierenrindenkarzinoms erschweren.
- Wir möchten aus diesen Erkenntnissen neue Strategien entwickeln, um Blutungen unter Mitotane zu vermeiden und die Therapie des Nebennierenrindenkarzinoms langfristig sicherer zu machen.
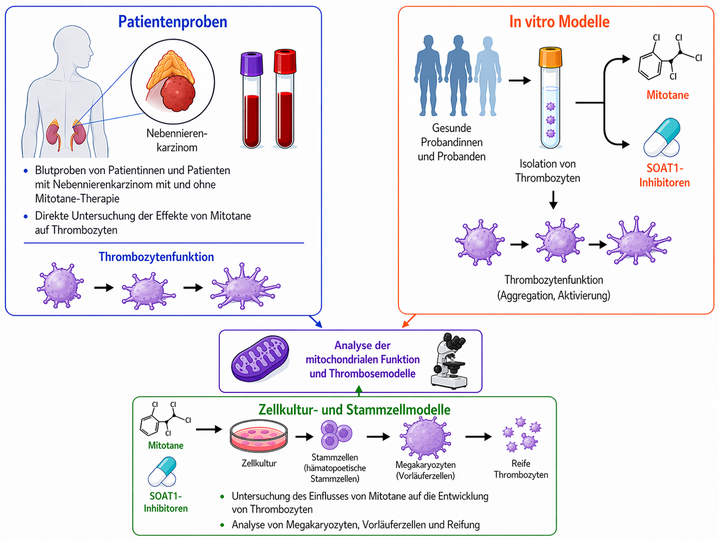
Abbildung 3: Study Design
Ansatz des Forschungsprojektes
Unser Projekt ist als translationales Forschungsprojekt angelegt, in welchem wir den Mechanismus der Blutungskomplikationen von Mitotane bei Patienten mit Nebennierenkarzinom entschlüsseln. Hierfür untersuchen wir einerseits Blutproben von Patientinnen und Patienten mit Nebennierenrindenkarzinom mit und ohne Mitotane-Therapie, um die Effekte von Mitotane auf die Thrombozyten bei den Patienten direkt zu untersuchen.
Andererseits isolieren wir Thrombozyten von gesunden Probanden und behandeln sie in vitro (im Reagenzglas) mit Mitotane und weiteren SOAT1-Inhibitoren, um die Effekte auf die Thrombozytenfunktion gezielt nachzustellen. Die Analyse der Mitochondrienfunktion und Zellatmung erfolgt in Zusammenarbeit mit dem Deutschen Zentrum für Herzinsuffizienz.
Ergänzend setzen wir Zellkultur- und Stammzellmodelle ein, um den Einfluss von Mitotane auf die Entwicklung von Thrombozyten zu untersuchen.
Welche Krebserkrankung soll behandelt werden?
Mit Hilfe unserer Forschung soll die Therapie des Nebennierenkarzinoms verbessert werden. Dadurch, dass die Medikamentengruppe der sogenannten SOAT1-Inibitoren, zu denen Mitotane gehört, gegenwärtig auch für die Therapie anderer Krebserkrankungen evaluiert wird, werden unsere Erkenntnisse auch hier von unmittelbarer Relevanz sein.
Warum soll das Forschungsprojekt unterstützt werden?
Unser Forschungsprojekt ist in dieser Form weltweit nur in Würzburg durchführbar, weil hier drei einzigartige Voraussetzungen zusammenkommen: Erstens das Würzburger Nebennierenkarzinom-Zentrum, das aufgrund seiner überregionalen Sichtbarkeit und Expertise zahlreiche Patientinnen und Patienten sowie Studien betreut und somit eine ausreichende Anzahl an Patienten für Untersuchungen rekrutiert. Zweitens die Würzburg Platelet Group am Institut für Experimentelle Biomedizin mit ihrer international sichtbaren Expertise in der Thrombozytenforschung. Drittens die hochspezialisierten Technologien zur Untersuchung der Mitochondrienfunktion und Zellatmung am Deutschen Zentrum für Herzinsuffizienz. Diese enge räumliche und wissenschaftliche Verzahnung ist entscheidend, da Thrombozyten aus Blutproben nach den derzeit bestehenden Leitlinien nur innerhalb von vier bis sechs Stunden nach der Blutabnahme verlässlich untersucht werden können.
Nur unter diesen infrastrukturellen Bedingungen lässt sich dieses bislang ungelöste klinische Problem nicht nur grundlagenwissenschaftlich aufklären, sondern gezielt mit dem Ziel bearbeiten, die Therapie von Patientinnen und Patienten mit Nebennierenrindenkarzinom konkret zu verbessern. Genau diese enge Verbindung von Innovation, klinischer Relevanz und unmittelbarem Nutzen für Betroffene zeichnet das Projekt aus.
- Nächstes
- Forschungsprojekte
- Vorheriges
