Zielgerichtete Aktivierung von TRAILR1 im 3D-Knochenmarkmodell zur Therapie des Multiplen Myeloms

Abbildung 1: Das Team von Dr. Isabell Lang und Dr. Dalia Sheta
TEAM
Unser interdisziplinäres Forschungsteam untersucht das Zusammenspiel von Tumorzellen und Mikroumgebung im Knochenmark beim Multiplen Myelom. Dieses komplexe System aus stromalen, endothelialen und immunologischen Zellen sowie der extrazellulären Matrix steuert maßgeblich Tumorwachstum, Immunflucht und Therapieresistenz.
Ziel unserer Arbeit ist es, die zugrunde liegenden Zell-Zell- und Zell-Matrix-Interaktionen sowie krankheitsrelevante Signalwege besser zu verstehen und therapeutisch nutzbar zu machen. Hierfür nutzen wir innovative 3D-Knochenmarkmodelle in Kombination mit modernen molekularen und bildgebenden Verfahren, die eine Analyse unter physiologisch relevanten Bedingungen ermöglichen – einschließlich der Integration primärer Patientenzellen. Parallel entwickeln und validieren wir neue, zielgerichtete Therapiestrategien, die Tumorzellen selektiv eliminieren und gleichzeitig Nebenwirkungen minimieren sollen.
Unser internationales Team am Universitätsklinikum Würzburg setzt sich aus promovierten Biologen und Medizinern zusammen und wird durch naturwissenschaftliche und medizinische Doktoranden, sowie technische Assistentinnen unterstützt – mit dem gemeinsamen Ziel, neue, spezifische und potenziell nebenwirkungsärmere Therapieformen beim Multiplen Myelom voranzutreiben.
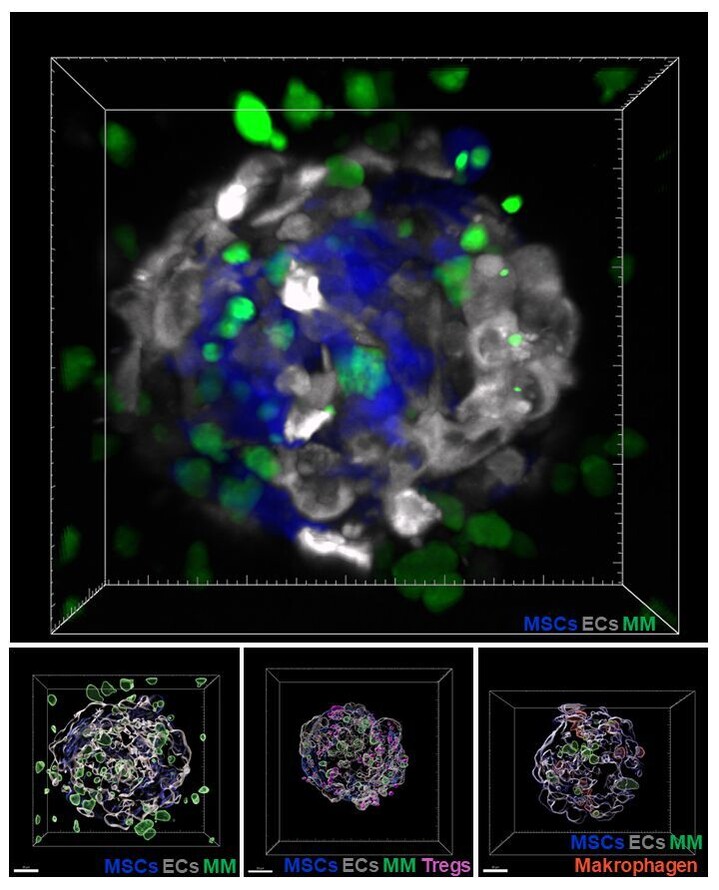
Abbildung 2: Konfokale Mikroskopie eines 3D-Myelom-(MM)-Sphäroids mit Integration von MM-Zellen in endotheliale Zellen (ECs) und mesenchymale Stromazellen (MSCs). Epifluoreszenzaufnahme des Sphäroids (oberes Panel). 3D-Oberflächenrendering einer z-Rekonstruktion, das zusätzlich die Integration von regulatorischen T-Zellen (Tregs) und Makrophagen innerhalb des Sphäroids zeigt (unteres Panel).
Motivation und Innovation
“Jeder Fortschritt beginnt mit einem besseren Verständnis der Krankheit. Mit unserem 3D-Modell kommen wir der Realität im Körper einen entscheidenden Schritt näher – damit wir Therapien entwickeln können, die Hoffnung geben und Leben verändern.”
Dr. Dalia Sheta
“Der Krebspatient steht für uns immer im Mittelpunkt. Unsere neuen Therapeutika müssen darauf abzielen die Behandlung effektiv und möglichst nebenwirkungsfrei zu machen.”
Dr. Isabell Lang
Das Multiple Myelom ist eine weiterhin unheilbare maligne Erkrankung des blutbildenden Systems, die trotz erheblicher therapeutischer Fortschritte durch häufige Rezidive und die Entwicklung von Resistenzen charakterisiert ist. Ein wesentliches Hindernis für die Erforschung der Krankheitsbiologie und die Entwicklung neuer Therapien ist die eingeschränkte Langzeitkultivierbarkeit primärer, patientenabgeleiteter Myelomzellen unter konventionellen in vitro Bedingungen.
Zur Überwindung dieser Limitation haben wir ein innovatives dreidimensionales (3D) Zellkulturmodell etabliert, das die Knochenmarkmikroumgebung des Multiplen Myeloms realitätsnah nachbildet (Abbildung 2). Ein zentrales Merkmal unseres Systems ist die gezielte Rekapitulation der extrazellulären Matrix (ECM) des Knochenmarks, einschließlich ihrer strukturellen, biochemischen und mechanischen Eigenschaften. In Kombination mit der Integration relevanter stromaler und tumorassoziierter Zelltypen ermöglicht dieses Modell eine physiologisch hochrelevante Untersuchung tumorspezifischer Prozesse, Zell-Zell- und Zell-Matrix-Interaktionen sowie therapiebedingter Adaptationsmechanismen. Damit stellt das System eine leistungsfähige Plattform für die präklinische Wirkstofftestung dar.
Wir entwickeln parallel dazu hoch aktive Wirkstoffe, die gezielt im Tumor wirksam werden und Krebszellen direkt ausschalten, z.B. über die Aktivierung des Todesrezeptors TRAIL (“TNF-related apoptosis inducing ligand”) -Rezeptor 1 (TRAILR1), ein Mitglied der TNF-Rezeptor-Superfamilie. Bisher zeigen konventionelle TRAIL-Rezeptor-Agonisten leider eine limitierte klinische Anwendbarkeit aufgrund dosislimitierender Toxizität, da sie nicht nur an den TRAILR1, sondern auch an den Todesrezeptor TRAILR2 (DR5) binden und diesen gleichzeitig aktivieren. Unsere neu entwickelten Nanobody-basierten TRAILR1-Agonisten ermöglichen hingegen ein effizientes und selektives Targeting von TRAILR1-sensitiven Tumoren, ohne Aktivierung von TRAILR2.
Hierfür wurden spezifische Nanobodies (Nbs) gegen den extrazellulären Teil von TRAILR1 generiert und durch multivalente Formate (3xNb:TRAILR1) sowie Fusion mit oligomerisierenden Proteingerüsten zu hochpotenten agonistischen Molekülen weiterentwickelt (Abbildung 3). Die gezielte Erhöhung der Valenz, d. h. die Steigerung der Anzahl an verfügbaren TRAILR1-Bindestellen, stellt dabei einen entscheidenden Mechanismus dar, um ansonsten nicht-agonistische anti-TRAILR1 Moleküle zu potenten Agonisten zu machen.
Um die Tumorspezifität noch weiter zu erhöhen, wurden bispezifische, konditional aktive Nb:TRAILR1-Fusionsproteine entwickelt, die eine effektive Rezeptoraktivierung nur bei gleichzeitiger Bindung an TRAILR1 und ein zweites Ankermolekül ermöglichen (Abbildung 3). Als Zielstrukturen dienen sowohl tumorspezifische Antigene wie BCMA und CD38 als auch Komponenten der Tumormikroumgebung, beispielsweise FAP. Darüber hinaus eröffnet die Kombination mit Immun-Checkpoint-gerichteten Nanobodies die Möglichkeit zur Entwicklung multifunktionaler Moleküle mit kombinierter apoptotischer und immunmodulatorischer Wirkung (z. B. CD70-gerichtete Ansätze).
Erste Daten aus 3D-Myelom-Sphäroidmodellen auf Basis etablierter Zelllinien belegen die hohe Wirksamkeit der entwickelten TRAILR1-Agonisten bei der Induktion von Apoptose. Im nächsten Schritt wird das System durch die Integration primärer Patientenzellen erweitert, um die klinische Relevanz weiter zu steigern und patientenspezifische Therapieansätze zu ermöglichen.
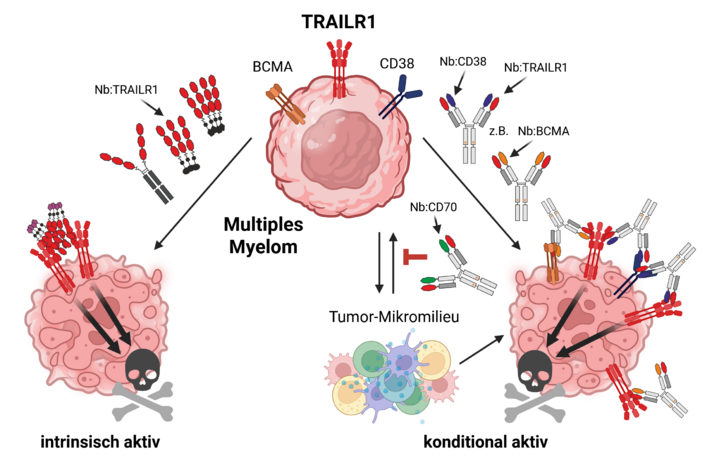
Abbildung 3: Wirkprinzip von intrinsisch aktiven (links) und konditional aktiven (rechts) Nanobody-basierten TRAILR1-Agonisten am Beispiel des Multiplen Myeloms. (Nb: nanobody)
Welche Ziele verfolgt das Projekt?
Ein zentrales Ziel dieses Projekts ist die Entwicklung und präklinische Validierung neuartiger, zielgerichteter Therapieansätze für das Multiple Myelom unter Nutzung eines physiologisch relevanten 3D-Knochenmarkmodells.
- Etablierung eines humanen 3D-Knochenmarkmodells, das die Knochenmarkmikroumgebung des Multiplen Myeloms einschließlich der extrazellulären Matrix (ECM) sowie relevanter stromaler, endothelialer und immunologischer Zellkomponenten realitätsnah rekonstruiert
- Integration primärer, patientenabgeleiteter Myelomzellen zur Abbildung patientenspezifischer Krankheitsheterogenität
- Untersuchung der TRAILR1/TRAILR2-Signalwege im Kontext der nativen Tumormikroumgebung
- Funktionelle Testung neuartiger Nanobody-basierter TRAILR1-Agonisten hinsichtlich ihrer Fähigkeit, selektiv Zelltod in Myelomzellen auszulösen
- Analyse konditional aktiver, bispezifischer TRAILR1-Agonisten im Kontext von tumor- und mikroenvironment-assoziierter Zielstrukturen (z. B. BCMA, CD38, FAP)
- Charakterisierung von Zell-Zell- und Zell-Matrix-Interaktionen, sowie deren Einfluss auf Therapieansprechen und Resistenzmechanismen
Langfristig strebt das Projekt die Entwicklung hochselektiver, patientenadaptierter Therapiestrategien an, die Tumorzellen effektiv eliminieren und gleichzeitig gesundes Gewebe möglichst schonen.
Ansatz des Forschungsprojektes
Das Projekt verfolgt einen translationalen Ansatz zur Entwicklung neuartiger Krebstherapeutika, die gezielt den programmierten Zelltod (Apoptose) in Tumorzellen induzieren. Im Gegensatz zu klassischen Strategien, die primär auf Immunaktivierung abzielen, fokussiert sich unser Ansatz auf die gezielte Aktivierung des TRAILR1-Signalwegs als therapeutische Schwachstelle des Multiplen Myeloms. TRAILR1, ein Todesrezeptor und Mitglied der TNF-Rezeptor-Superfamilie, kann bei selektiver Aktivierung Apoptose in Tumorzellen auslösen, während gesunde Zellen weitestgehend verschont bleiben.
Zur realitätsnahen Untersuchung dieser Mechanismen nutzen wir ein innovatives 3D-Knochenmarkmodell, das die komplexe Tumormikroumgebung des Multiplen Myeloms nachbildet. Besonders hervorzuheben ist die Rekonstruktion der extrazellulären Matrix (ECM), die eine zentrale Rolle für Zelladhäsion, Signalübertragung und Therapieresistenz spielt. Auf dieser Plattform werden neuartige Nanobody-basierte TRAILR1-Agonisten getestet, die eine hohe Rezeptorspezifität besitzen und eine unerwünschte Aktivierung des TRAILR2 vermeiden. Ein besonderer Schwerpunkt liegt auch auf der Entwicklung bispezifischer, konditional aktiver Moleküle, die nur dann wirksam werden, wenn sie gleichzeitig an TRAILR1 und ein zweites Zielmolekül auf der Krebszelle selbst oder in der Tumorumgebung binden. Dadurch wird eine hochselektive Aktivierung direkt im Tumorgewebe ermöglicht.
Nach erfolgreichen Vorarbeiten mit Zelllinien erfolgt nun die Erweiterung auf primäre Patientenzellen, um die klinische Relevanz der Ergebnisse zu erhöhen und patientenspezifische Therapieantworten zu untersuchen. Ziel des Ansatzes ist die Identifikation und Validierung neuer therapeutischer Strategien, die eine präzise, wirksame und möglichst nebenwirkungsarme Behandlung des Multiplen Myeloms ermöglichen.
Welche Krebserkrankung soll behandelt werden?
Zunächst steht das Multiple Myelom im Fokus des Projekts. Diese maligne Erkrankung des blutbildenden Systems ist trotz signifikanter Fortschritte in der Therapie weiterhin nicht heilbar und zeichnet sich insbesondere durch häufige Rezidive sowie die Entwicklung von Therapieresistenzen aus. Ziel ist es, neue, präzisere und besser verträgliche Behandlungsstrategien für diese Patientengruppe zu entwickeln.
Warum soll das Forschungsprojekt unterstützt werden?
Das Projekt vereint mehrere innovative Ansätze, die einen hohen translationalen und klinischen Mehrwert erwarten lassen: Im Zentrum steht die Entwicklung neuartiger Nanobody-basierter TRAILR1-Agonisten, die eine selektive Induktion von Tumorzelltod ermöglichen und dabei eine verbesserte Spezifität gegenüber bisherigen TRAIL-basierten Ansätzen aufweisen. Ergänzend werden erstmals konditional aktive, bispezifische Moleküle eingesetzt, die eine gezielte Aktivierung ausschließlich in der Tumormikroumgebung erlauben.
Ein weiterer zentraler Innovationsaspekt ist die Nutzung eines hochrealistischen 3D-Knochenmarkmodells, das nicht nur die zelluläre Zusammensetzung, sondern insbesondere auch die extrazelluläre Matrix (ECM) des Knochenmarks nachbildet. Dieses System erlaubt eine deutlich präzisere Abbildung der in vivo Situation als konventionelle 2D-Kulturen. Darüber hinaus werden primäre, patientenabgeleitete Myelomzellen eingesetzt, um die klinische Relevanz der Ergebnisse zu erhöhen und patientenspezifische Therapieantworten zu untersuchen.
Durch die Kombination dieser Ansätze schafft das Projekt eine innovative präklinische Plattform, die sowohl ein besseres Verständnis der Tumorbiologie ermöglicht als auch die Entwicklung neuer, zielgerichteter und potenziell nebenwirkungsärmerer Therapieformen vorantreiben kann.
- Nächstes
- Forschungsprojekte
- Vorheriges
