Biologische Zeit & Tumoradaption–endokrine Zeitgeber als Schlüssel zur Immuntherapie

Abbildung 1: Teamfoto der Arbeitsgruppe
verortet an den Lehrstühlen für zelluläre Immuntherapie (Leitung: Prof. M. Hudecek), der Medizinischen Klinik & Poliklinik II (Leitung: Prof. H. Einsele) sowie dem Lehrstuhl für Endokrinologie & Diabetologie (Leitung: Prof. M. Fassnacht) am Universitätsklinikum Würzburg. v.links n. rechts: Alesia Scholl, Chloé Georges, Esther Adeyemo, Marc P. Schauer (fehlend Felix Meindl kl. Bild)
Marc P. Schauer ist Doktorand an den Lehrstühlen für Endokrinologie und zelluläre Immuntherapie, ist angehender Assistenzarzt und NCT Clinical Trialist in der Medizinischen Klinik II und Leiter und Ideengeber des Projektes.
Esther Adeyemo ist eine Master-Studentin, Chloé Georges, Alesia Scholl und Felix Meindl sind als TAs der Laborgruppenkollaboration eine essentielle laborexperimentelle Stütze.
TEAM
Wir beschäftigen uns mit der Erforschung neuer Mechanismen der Tumor-Immunevasion. Dabei verbinden wir Grundlagenforschung zu hormonellen Signalwegen und biologischen Rhythmen mit translationalen Ansätzen der Krebsimmuntherapie insbesondere der Immuncheckpointinhibitoren und CAR-T Zelltherapie. Ziel ist es, dynamische Anpassungsstrategien von endokrin-aktiven Tumoren besser zu verstehen und daraus neue therapeutische Konzepte abzuleiten.

Abbildung 2: MACS Quant Miltenyi (links), WesternBlot-Gerät (rechts)
Motivation und Innovation
„Jahrzehntelang haben wir Tumore zu einem einzigen Moment biopsiert, sequenziert und charakterisiert – diese statische Betrachtungsweise berücksichtigt jedoch nicht, welche Hormone zu welcher Tageszeit, Zyklusphase oder in Stressphasen zirkulieren. Unser Ziel ist es, aus dem Standbild einen Film zu machen, um endlich zu verstehen, was zwischen den Aufnahmen passiert.“
Die Fähigkeit von Tumoren, der Immunüberwachung zu entgehen, stellt eine zentrale Herausforderung moderner Krebstherapien dar. Während genetische Veränderungen und Signale aus dem Tumormikromilieu intensiv erforscht wurden, blieb eine mögliche zeitliche Dimension der Tumorantigenität bislang weitgehend unbeachtet. Zirkadiane endokrine Rhythmen steuern zahlreiche physiologische Prozesse – von Stoffwechsel und Hormonfreisetzung bis hin zu Immunfunktionen. Eigene Vorarbeiten unserer Arbeitsgruppe, die u.a. mit dem Schöller-Junkmann-Preis der Deutschen Gesellschaft für Endokrinologie sowie dem Young Scientists IO Award von Bristol Myers Squibb in Kooperation mit der Deutschen Krebsgesellschaft ausgezeichnet wurden, konnten zeigen, dass Glukokortikoide Tumorantigene aktiv modulieren und das Therapieansprechen beeinflussen können.
Auf dieser Grundlage verfolgen wir die innovative Hypothese, dass Tumoren biologische Zeitgeber aktiv nutzen, um ihre Erkennbarkeit durch das Immunsystem über den Tagesverlauf dynamisch zu regulieren. Ein besonderer Fokus liegt auf Glukokortikoiden, deren täglich oszillierende, pulsatile Freisetzung starke Effekte auf Immunantworten besitzt und die durch intratumorale Enzyme lokal moduliert werden können. Ergänzend möchten wir geschlechtsspezifische Unterschiede adressieren und die im Rahmen des Menstruationszyklus modulierten Sexhormone in ihrer immunologischen Wirkung näher charakterisieren.

Abbildung 3: LC-MS Massenspektrometrie-Einheit
Welche Ziele verfolgt das Projekt?
Ziel des Projektes ist es im ersten Schritt zu klären, ob Tumoren im Tagesverlauf ihre Antigenpräsentation und immunologische Sichtbarkeit verändern. Wir untersuchen, ob die intratumorale Glukokortikoid-Metabolisierung eine Art „endokrine Tumoruhr“ etabliert, die Immunerkennung, angeborene Immunaktivierung sowie das Ansprechen auf Immuntherapien rhythmisch beeinflusst. Langfristig sollen diese Erkenntnisse dazu beitragen, zeitlich optimierte Therapieansätze zu entwickeln und neue Biomarker für das Therapieansprechen zu identifizieren, die gleichermaßen genutzt werden können chronotherapeutisch durchgeführte IIT-Studien am Würzburger Standort in soliden Tumoren durchzuführen. Im zweiten Schritt wollen wir diese Erkenntnisse um Sexualhormone erweitern, um geschlechtsspezifische Unterschiede genauer zu untersuchen und unterschiedliches Ansprechen auf Immuntherapien in Mann und Frau weiter zu differenzieren. Dies beinhaltet u.a. die hormonellen Veränderungen im Rahmen des weiblichen Monatszyklus sowie der geschlechtsspezifischen Wechseljahre.
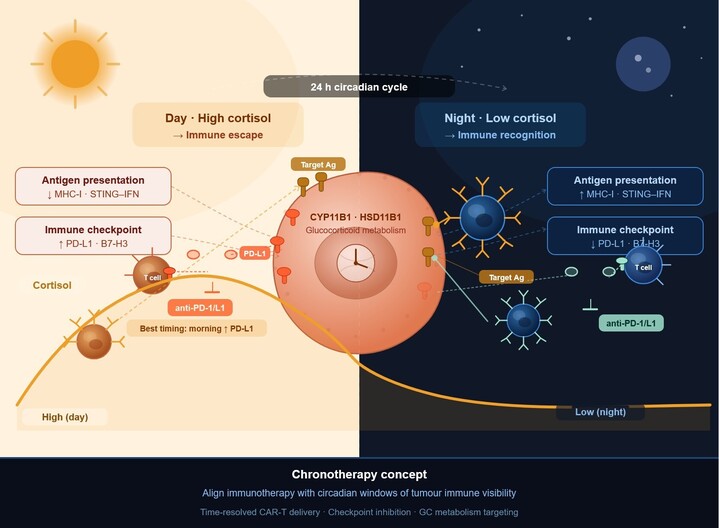
Abbildung 4: Graphical abstract, Circadian tumour immune visibility gated by glucocorticoid metabolism
Ansatz des Forschungsprojektes
Das Projekt kombiniert synchronisierte Tumorzellmodelle, in-vitro Untersuchungen, funktionelle Hormon- und Immunassays, genetische Knockout-Modelle sowie in-vivo-Untersuchungen in präklinischen Mausmodellen. Dabei wird analysiert, wie Enzyme des Glukokortikoid-Metabolismus, insbesondere HSD11B1 und CYP11B1, systemische hormonelle Rhythmen im Tumor verstärken oder autonom modulieren können. Ein zentraler Bestandteil ist die Untersuchung, ob tumorassoziierte Antigenstrukturen im Tages- bzw. Monatszyklusverlauf schwanken. Da Antigene in der klinischen Praxis meist nur zu einem einzelnen OP-Zeitpunkt bestimmt werden, könnten zeitliche Veränderungen bislang unentdeckt bleiben, zusätzliche Zielstrukturen identifizieren und zur variablen Wirksamkeit von Immuntherapien beitragen.
Welche Krebserkrankung soll behandelt werden?
Der Schwerpunkt liegt auf soliden Tumoren des Gastrointestinaltraktes wie dem Nebennierenrindenkarzinom, dem Bauchspeicheldrüsen-, Magen-, Darm- und Brustkrebs, bei denen Immuntherapien bislang nur begrenzten Erfolg zeigen. Die zugrunde liegenden Mechanismen könnten jedoch auch für andere Tumorentitäten von Bedeutung sein, in diesem Zuge finden sich bereits Kollaborationen am Würzburger Standort bspw. der Dermatologie.
Warum soll das Forschungsprojekt unterstützt werden?
Immuntherapien haben die Krebsmedizin grundlegend verändert, dennoch profitieren viele Patientinnen und Patienten nicht oder nicht dauerhaft von diesen Behandlungen. Das Projekt adressiert eine bislang wenig erforschte Dimension der Tumorbiologie: zum einen die zeitabhängige Regulation der Tumorantigenität als auch die sexspezifischen Unterschiede in der Tumorgenese und dem Therapieansprechen. Durch ein besseres Verständnis zirkadianer hormoneller Signalwege könnten neue Strategien entstehen, um Immuntherapien gezielter einzusetzen, Therapieresistenzen zu überwinden und langfristig die Behandlungsergebnisse zu verbessern.
- Nächstes
- Forschungsprojekte
- Vorheriges
