Stärkung der Immunantwort gegen das Multiple Myelom durch gezielte Aktivierung

Abbildung 1: Das interdisziplinäre Forschungsteam der Medizinischen Klinik II untersucht Schlüsselmechanismen der körpereigenen Immunantwort gegen Krebs und entwickelt neue Strategien zu deren therapeutischen Nutzung.
TEAM
Unser interdisziplinäres Team vereint langjährige klinische und wissenschaftliche Expertise in der Krebsforschung und -behandlung. Unter der Leitung von Prof. Dr. Dr. Beilhack und Prof. Dr. rer. nat. Wajant arbeiten wir an der Schnittstelle zwischen Labor und Klinik mit dem Ziel, neue und wirksamere Therapien für Krebserkrankungen zu entwickeln. In unserer Arbeit nutzen wir Patientenproben in hochentwickelte 3D-Zellkultursysteme als auch präklinische in-vivo-Modelle, selche die komplexen Bedingungen im menschlichen Körper realitätsnah abbilden, um innovative immunologische Konzepte und neuartige Protein-Therapeutika zu entwickeln.
Wir untersuchen nicht nur, wie Krebs entsteht und Therapien versagen. Auf dieser Grundlage entwickeln wir innovative immunologische Ansätze und neuartige Proteintherapeutika, um die Wirksamkeit moderner Krebsbehandlungen gezielt zu verbessern.

Abbildung 2: Prof. Dr. Dr. Andreas Beilhack (links) & Prof. Dr. rer. nat. Harald Wajant (rechts)
Motivation und Innovation
„Warum wirken viele Krebsmedikamente im Labor, aber nicht beim Patienten?“
Diese Frage steht im Zentrum unserer Forschung. Krebszellen im Körper erzeugen sich eine eigene vorteilhafte Umgebung, das sogenannte Tumormikromilieu, die aktiv vor einer Attacke des Immunsystems schützt. Nicht nur bei soliden Tumorerkrankungen, auch beim Multiplen Myelom, einer Krebserkrankung des Knochenmarks, bildet diese Umgebung eine Art Schutzschild, der Therapien deutlich weniger wirksam macht. In klassischen Laborexperimenten wachsen Krebszellen meist isoliert auf flachen Oberflächen. Doch im menschlichen Körper sind sie in ein komplexes Netzwerk aus verschiedenen Zelltypen, eben dem Tumormikromilieu, eingebettet. Um diese Realität besser abzubilden, haben wir ein neuartiges dreidimensionales Modell entwickelt, das das Knochenmark, in dem sich das MM manifestiert, möglichst realistisch nachahmt und mit Myelomzellen besiedelt wird. In diesem Modell zeigen sich Krebszellen deutlich widerstandsfähiger gegenüber Therapien, insbesondere auch T-Zell-Therapien – genau wie im Patienten.
Unsere Innovation besteht darin, dieses realitätsnahe Modell zu nutzen, um Therapiestrategien zu entwickeln, die die immunsupprimierende Wirkung des Tumormikromilieus durchbrechen. Damit T-Zellen Krebszellen wirksam bekämpfen können, benötigen sie drei entscheidende Aktivierungssignale: ein Erkennungssignal, das den Tumor identifiziert, ein Verstärkungssignal und schließlich ein drittes Signal, das über die Stärke, Ausdauer und Qualität der Immunantwort entscheidet.
Gerade dieses dritte Signal fehlt im Tumormilieu häufig oder ist zumindest nur unzureichend suboptimal verfügbar. Die Folge: T-Zellen verlieren an Kraft, erschöpfen („Exhaustion“) und können den Krebs nicht mehr effektiv kontrollieren. Dieses entscheidende dritte Signal wird über eine spezielle Gruppe von Rezeptoren auf T-Zellen vermitteltm, die zur sogenannten TNF-Rezeptor-Superfamilie gehören (TNFRSF) gehören und eine zentrale Rolle bei der Verstärkung und Aufrechterhaltung der Immunantwort spielen.
Hier setzen wir an. Wir haben neue, besonders wirksame Aktivatoren für diese TNFRSF-Rezeptoren entwickelt, die wie ein gezielter „Energieschub“ für das Immunsystem wirken: Sie stärken die Ausdauer der T-Zellen, erhöhen ihre Schlagkraft und helfen ihnen, auch unter den schwierigen Bedingungen in den Tumor einzudringen und im Tumor aktiv zu bleiben. Vereinfacht gesagt geben wir den Immunzellen genau die Impulse, die sie über ihre prinzipielle Aktivierung durch die Signale 1 und 2 brauchen, um den Krebs nachhaltig zu bekämpfen.
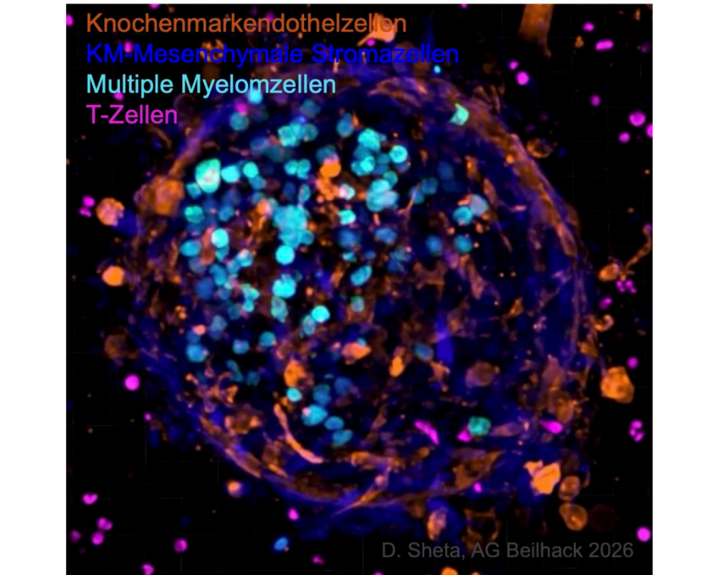
Abbildung 3: Unsere 3D-Knochenmark-Myelom-Modelle bilden den Tumor eines Patienten realitätsnah nach und ermöglichen es uns, zu prüfen, welche unserer neuen TNFRSF-Aktivatoren bzw. welche Kombination dieser Aktivatoren am besten geeignet ist, um die antitumorale Wirkung von T-Zellen optimal zur Entfaltung zu bringen; ein entscheidender Schritt hin zu wirksameren Therapien für Patientinnen und Patienten
Welche Ziele verfolgt das Projekt?
Das Ziel unseres Projekts ist es, die körpereigene Immunabwehr, insbesondere T-Zellen, so zu stärken, dass sie Krebszellen auch im immunsuppressiven schützenden Umfeld des Tumormikromilieus effektiv erkennen und zerstören können. Wir möchten erreichen, dass moderne Immuntherapien wie BiTEs oder CAR-T-Zellen ihre volle Wirkung entfalten können, selbst unter den schwierigen Bedingungen des speziellen Tumormikromilieus im Knochenmark.
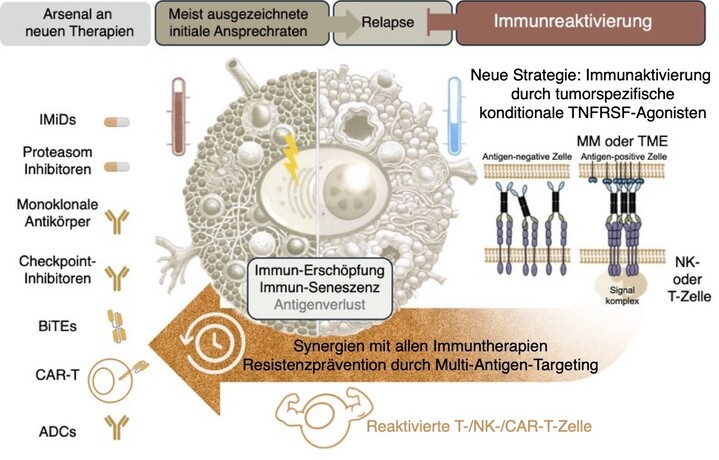
Abbildung 4: Trotz moderner Therapien kommt es beim Multiplen Myelom häufig zu Rückfällen, da das Immunsystem zunehmend geschwächt und erschöpft ist. In diesem Projekt nutzen wir neuartige von uns entwickelte TNFRSF-Aktivatoren, die gezielt Krebszellen erkennen und gleichzeitig T-Zellen wieder aktivieren, mit dem Ziel, die körpereigene Abwehr nachhaltig gegen den Tumor zu stärken.
Ansatz des Forschungsprojektes
In unserem Projekt nutzen wir patienteneigene Myelomzellen und kombinieren sie mit unterstützenden Zellen des Knochenmarks in einem dreidimensionalen Zellkultursystem, das die Situation im Körper realitätsnah abbildet. In dieses Modell integrieren wir gezielt verschiedene T-Zellen die natürlicherweise oder therapeutisch induziert bzw. verabreicht antitumoral wirksam sein können: Myelom-reaktive T-Zellen, durch sogenannte BiTEs aktivierte T-Zellen, natürliche Killerzellen sowie moderne CAR-T-Zellen – also speziell ausgestattete Immunzellen, die Krebszellen präzise erkennen und angreifen können.
Der entscheidende Innovationsschritt ist der Einsatz unserer neu entwickelten TNFRSF-Aktivatoren. Diese wirken wie ein gezielter Verstärker der Immunantwort: Sie steigern die Schlagkraft, Ausdauer und Widerstandsfähigkeit der T-Zellen und helfen ihnen, die Schutzmechanismen des Tumors zu überwinden. Wir möchten so die Wirksamkeit moderner Immuntherapien direkt in einer realitätsnahen Tumorumgebung verbessern – und gezielt Strategien entwickeln, die auch im Patienten vorteilhaft funktionieren.
Welche Krebserkrankung soll behandelt werden?
Im Mittelpunkt unserer Forschung steht das Multiple Myelom. Trotz großer Fortschritte in der Therapie bleibt diese Erkrankung für viele Betroffene nicht heilbar. Rückfälle sind häufig und stellen eine große Herausforderung dar.
Die Bedeutung unseres Ansatzes geht jedoch über diese Erkrankung hinaus. Auch bei vielen anderen Krebsarten, insbesondere bei soliden Tumoren wie Lungen-, Brust-, Darm- oder Bauchspeicheldrüsenkrebs, spielt die Tumorumgebung eine entscheidende Rolle für das Versagen von Therapien. Die Erkenntnisse aus unserem Projekt könnten daher helfen, die Behandlung vieler Krebserkrankungen grundlegend zu verbessern.
Warum soll das Forschungsprojekt unterstützt werden?
Dieses Projekt greift ein zentrales Problem der Krebsmedizin auf: Vielversprechende Therapien, Tumor-spezifische Immunzellen nutzen, verlieren im menschlichen Körper oft an Wirksamkeit. Unsere Forschung setzt genau an diesem Punkt an und versucht, die Gründe dafür zu überwinden. Mit unserem neuartigen 3D-Modell können wir Therapien unter Bedingungen testen, die der Realität im Patienten sehr nahekommen. Gleichzeitig entwickeln wir neue Strategien, um das Immunsystem gezielt zu stärken und so die Wirksamkeit moderner Behandlungen zu verbessern.
Ihre Unterstützung ermöglicht es uns, diesen vielversprechenden Ansatz weiterzuverfolgen und den nächsten Schritt in Richtung besserer, nachhaltiger Krebstherapien zu gehen. Unser Ziel ist es, Patientinnen und Patienten langfristig bessere Heilungschancen und eine höhere Lebensqualität zu ermöglichen.
- Nächstes
- Forschungsprojekte
- Vorheriges
