Nachweis von Immunzellbotenstoffen gegen Covid-19 für die Diagnostik und Impfstofftestung
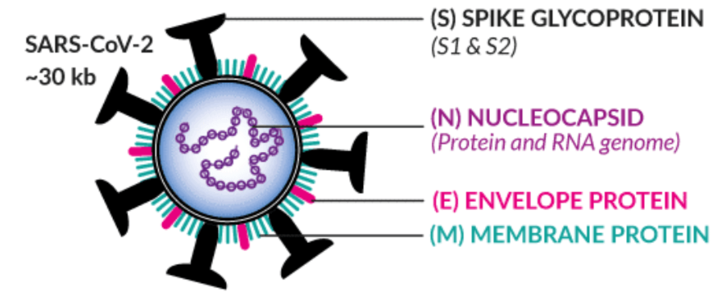
Abbildung 1
Schematische Abbildung des SARS-CoV-2 Virus (“Coronavirus”). Die Reaktion des Immunsystems auf Teile der Viruseiweiße S, N und M sollen untersucht werden und eine Differenzierung von Covid-19 positiven und negativen Patient/-innen zulassen (Quelle der Abbildung: https://www.invivogen.com/spotlight-covid-19-infection).
Team
In der AG Loeffler (Labor WÜ4i, www.wue4i.org) arbeiten unter der Leitung von Herrn Prof. Dr. Jürgen Löffler derzeit 15 Mitarbeiter/-innen, darunter drei Postdoktoranden/-innen, vier Doktoranden/-innen und vier technische Assistenten/-innen. Der wissenschaftliche Schwerpunkt unserer Arbeitsgruppe liegt in der molekularen und immunologischen Analyse von humanpathogenen Pilzinfektionen bei hämato-onkologischen Patienten/-innen. Im Speziellen fokussieren wir uns auf die Hochrisikogruppe der Patienten nach allogener Blutstammzelltransplantation. Unsere Expertise sehen wir in der Entwicklung von diagnostischen Verfahren für diese Patienten/-innen und in der Analyse der Immunantwort gegen opportunistische Pilzerreger. Unsere Gruppe ist seit 2006 maßgeblich an der Entwicklung des molekularen Nachweises (PCR) von invasiven Pilzinfektionen bei onkologischen Patienten/-innen beteiligt, welcher inzwischen weltweit in standardisierter Form angewendet wird. Herr Professor Löffler ist auf Grund seiner jahrelangen Expertise nun der Vorsitzende des Vorstands der Fungal PCR Initiative (FPCRI, www.fpcri.eu), eine Arbeitsgruppe der International Society for Human and Animal Mycology (https://www.isham.org/working-groups/european-aspergillus-pcr-initiative-eapcri).
Darüber hinaus haben wir für das Uniklinikum Würzburg hochsensitive molekulare Nachweisverfahren für die so genannte Chimärismusanalyse etabliert und evaluiert, womit inzwischen am UKW bei hunderten von Patienten nach allogener Stammzelltransplantation der patientenspezifische Verlauf der Transplantation überwacht wird. Die Arbeitsgruppe von Herrn Professor Löffler hat für Ihre Arbeiten bereits mehrere Millionen Euro an Drittmitteln eingeworben, u. a. von der EU (FP6), der DFG (SFB TR124 FungiNet), dem ERANET (aspBiomics), vom BMBF (Art4FUN), sowie vom Bayerischen Staatsministerium (TbaseIA). Herr Professor Löffler ist Autor / Ko-Autor von 180 Publikationen.
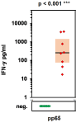
Abbildung 2
Vollblut Proben von 8 Cytomegalovirus (CMV)-negativen (grün) und 8 CMV positiven (rot) Patienten nach Stammzelltransplantation (60-180 Tage nach Transplantation) wurden für 24 h mit Teilen des Eiweißes pp65 von CMV stimuliert. Die Konzentration in der zellfreien Fraktion des Bluts (Plasma) des Botenstoffs IFN-γ wurde anschließend mittels ELISA quantifiziert. Der VB-ELISA war in der Lage beide Gruppen in den getesteten Patienten verlässlich zu unterscheiden.
Motivation und Innovation der Arbeitsgruppe
Unsere weitreichenden Erfahrungen in der Entwicklung von diagnostischen Verfahren für verschiedene Infektionserreger haben wir in den letzten Jahren auch für die Entwicklung von optimierten Testsystemen zur funktionellen Analyse der Immunzell-Antwort auf Pilze und Viren genutzt.
Wir haben u. a. kürzlich ein Vollblut-Stimulationssystem für Botenstoffanalysen mittels einem so genannten „ELISA-Verfahren“ („VB-ELISA“) entwickelt.
Hierbei wird Blut des Patienten mit hochspezifischen kleinen Eiweißbestandteilen („Antigene“) eines definierten Krankheitserregers stimuliert. Für dieses System haben wir die Stimulationsbedingungen der Zellen deutlich verbessert, um auch schwächere Signale messen zu können. Bei Patienten/-innen nach allogener Stammzelltransplantation gelang es uns bereits mittels VB-ELISA zuverlässig, Patienten/-innen mit Cytomegalovirus (CMV) Infektion von nicht-infizierten Patient/-innen zu unterscheiden (Abbildung 2). Mit dieser Methode werden hauptsächlich T-zelluläre (ein Zelltyp der weißen Blutkörperchen) Antworten analysiert. Es konnte aktuell in einer Arbeit der Charité Berlin (Braun et al., 2020) gezeigt werden, dass auch in Covid-19 Patienten diese Antworten gemessen werden können. Bei SARS-CoV (2002/2003) ging eine stärkere T-zelluläre Antwort mit verbesserten Krankheitsverläufen einher. Durch die strukturellen Ähnlichkeiten ist es wahrscheinlich, dass dies auch auf SARS-CoV-2 zutrifft. Aufgrund der vielversprechenden Vorergebnisse und unserer Erfahrung in der Optimierung von immunzellulären Methoden gehen wir davon aus, dass unsere neuartige Methode auch rasch, zuverlässig und reproduzierbar für weitere Krankheitserreger adaptiert werden kann und insbesondere auch bei Covid-19 Patienten/-innen erfolgreich eingesetzt werden kann (Abbildung 3).
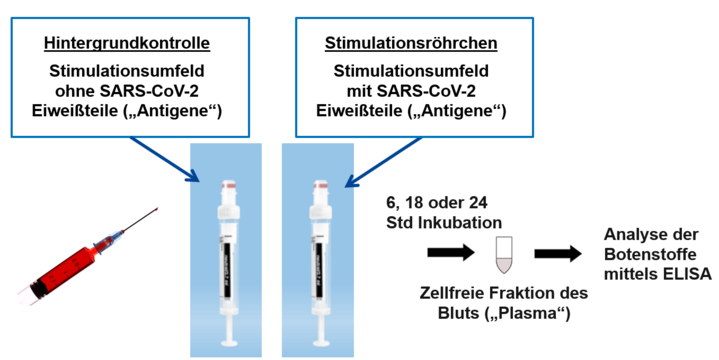
Abbildung 3
Covid-19 Stimulationsröhrchen enthalten im Gegensatz zu den Röhrchen der Hintergrundkontrolle verschiedene definierte Bestandteile eines SARS-CoV-2 („Coronavirus“) Eiweißes. Nach Inkubation wird die zellfreie Fraktion des Blutes („Plasma“), in der sich die Botenstoffe messen lassen, abgenommen und die Konzentration der Botenstoffe wird quantifiziert. Zellen von Patienten mit akuter oder zurückliegender SARS-CoV-2 Infektion erkennen die Eiweiße des Virus („Antigene“) wieder und schütten mutmaßlich daraufhin eine größere Menge von bestimmten Botenstoffen aus als Zellen von Patienten, bei denen noch nie eine SARS-CoV-2 Infektion vorlag. Wir erhoffen uns hierdurch Rückschlüsse auf das Krankheitsgeschehen und die Ausbildung der Immunantwort bei Patienten mit Covid-19.
Projektziele
Der VB-ELISA soll spezifisch für Covid-19 Patienten/-innen im Rahmen einer Pilotstudie etabliert, evaluiert und validiert werden. Es sollen die folgenden Hypothesen überprüft werden:
- Der VB-ELISA bietet eine verlässliche Plattform zur Detektion T-zellulärer Antworten für die Planung und Verlaufskontrolle zukünftiger Covid-19 Impfstudien.
- Der VB-ELISA kann eine zurückliegende Coronavirus Infektion früher und langanhaltender feststellen als ein Antikörpertest.
- Der VB-ELISA kann spezifische immunbiologische Unterschiede zwischen mit Covid-19 infizierten Krebspatient/-innen mit Leukämien oder Lymphomen und nicht-onkologischen Patient/-innen verlässlich definieren.
Ansatz des Forschungsprojektes
Der VB-ELISA wird mit Eiweißbestandteilen von SARS-CoV-2 angereichert und auf diese Virusbestandteile hin optimiert. Anschließend sollen die Reaktionen verschiedener Patienten- und Kontrollgruppen charakterisiert und miteinander verglichen werden, um die Funktionalität und Empfindlichkeit des Tests zu untersuchen.
Die gewonnenen Proben werden auf 23 verschiedene Botenstoffe hin analysiert und miteinander verglichen. Hierdurch kann die Immunantwort auf Covid-19 detailliert charakterisiert und ein Botenstoff oder eine Botenstoffkombination, die eine Unterscheidung von infizierten und nicht infizierten Individuen leisten kann, gefunden werden. Parallel zu unserem VB-ELISA sollen Antikörpertests durchgeführt werden, um die Leistungsfähigkeit unseres Tests zu vergleichen.
Krebserkrankung, die behandelt werden soll
Onkologische Patient/-innen gehören u. a. laut Definition des Robert Koch-Instituts zu den SARS-CoV-2 Risikogruppen. Daher sind diese Patienten/-innen besonders abhängig von einer verlässlichen multi-modalen Diagnostik (bei Covid-19 neben der klassischen molekularen Diagnostik zusätzlich Alternativen, wie diese neu entwickelte T-Zell basierte Diagnostik). Zudem ist es relevant, insbesondere in diesem Patientenkollektiv, nach dem ein Impfstoff gegen Coronaviren entwickelt werden konnte, auch einen entsprechenden Impferfolg verlässlich dokumentieren zu können. Durch eine sehr realistische Nachahmung der Prozesse im menschlichen Körper mittels unseres Tests könnten zukünftig vielversprechende von weniger vielversprechenden Impfstoffen unterschieden werden, wodurch die Entwicklung von Covid-19 Impfstrategien speziell für onkologische Patienten/-innen beschleunigt werden würde. Die Charakterisierung der Immunantwort von onkologischen Patienten/-innen könnte außerdem neue Therapieansätze speziell für diese Patientengruppe hervorbringen. Des Weiteren könnten Erkenntnisse aus dieser Studie wiederum in zukünftige Projekte für weitere opportunistische Infektionen bei Patienten/-innen nach Krebserkrankung (z. B. für Adenoviren) einfließen.
Warum soll das Forschungsprojekt unterstützt werden?
Durch eine sehr realistische Abbildung der Prozesse im menschlichen Körper bei einer Covid-19 Infektion könnte unser Test die Entwicklung von Therapieoptionen und Impfstoffen vereinfachen und verbessern. Dies ist insbesondere wichtig für bestimmte Covid-19 Hoch-Risikogruppen, wie Krebspatienten/-innen. Des Weiteren besteht die berechtigte Hoffnung, dass unser Test zusätzlich auch in der Lage ist, zurückliegende Infektionen von SARS-CoV-2 und anderen grippalen Coronaviren, die potenziell eine schützende Reaktion des Immunsystems gegen SARS-CoV-2 hervorrufen könnten, schneller und langanhaltender als die zurzeit verwendeten Antikörpertests detektieren zu können. Auf Grundlage dessen könnten Schutzmaßnahmen für besondere Risikogruppen besser gesteuert werden.
Schließlich bleibt anzumerken, dass von einer zukünftigen, so genannten 2. Welle an Patient/-innen mit Covid-19 Infektionen ausgegangen werden muss. Bei dieser Welle könnte u. U. sogar eine größere Anzahl an Patient/-innen betroffen sein. In solch einem Szenario sind daher zwangsläufig wiederum insbesondere Patient/-innen mit Krebs in das Studiengeschehen einzuschließen. Dabei soll dann im Vordergrund stehen, mit unserer Methode solche Krebspatienten/innen zu identifizieren, die bereits eine Infektion mit Covid-19 durchgemacht haben, bzw. in der Zukunft solche Krebspatient/-innen zu überwachen, die bereits gegen Covid-19 geimpft wurden und bei denen die Frage im Raum steht, ob ihre Impfung erfolgreich verlief und damit Schutz gegen Covid-19 bieten kann.
