ECM-Anker zur lokalen Steuerung der Immunantwort im Melanom

Abbildung 1: Mitglieder der AG Schmieder, Prof. Dr. med. Astrid Schmieder (AG Leiterin, dritte von rechts)
TEAM
In der Arbeitsgruppe um Prof. Dr. med. Schmieder erforschen junge Mediziner:innen und Naturwissenschaftler:innen die Biologie der Makrophagen, insbesondere auch im Zusammenhang mit Hautkrebs. Ihr Ziel ist es, deren bisher eher negative Wirkung auf Immuntherapien so zu verändern, dass sie die Behandlung künftig unterstützen.
Motivation und Innovation
„Obwohl Immuntherapien die Behandlung von Hautkrebs deutlich verbessert haben, sprechen noch immer etwa die Hälfte der Patientinnen und Patienten nicht darauf an.“
Prof. Dr. med. Astrid Schmieder
Das Projekt setzt genau an diesem Punkt an: Es soll eine Lösung für die bisher nachteilige Wirkung von tumorassoziierten Makrophagen (TAMs) gefunden werden.
Herangehensweise - Die Arbeitsgruppe verfolgt einen neuen und kreativen Ansatz. Statt den Tumor direkt anzugreifen, wird das Umfeld des Tumors (das sogenannte Tumormikromilieu) gezielt verändert. TAMs, die eigentlich den Tumor bekämpfen sollten, werden dabei so „umprogrammiert“, dass sie ihre ursprüngliche Schutzfunktion wieder aufnehmen.
Innovation - Besonders innovativ ist dabei der Einsatz von maßgeschneiderten Wirkstoff-Konstrukten (Biokonjugaten). Diese bringen ein Medikament gezielt in die Nähe des Tumors und setzen es genau dort frei, wo es gebraucht wird.
Vorteil - Dadurch kann die Behandlung wirksamer und gleichzeitig schonender werden.
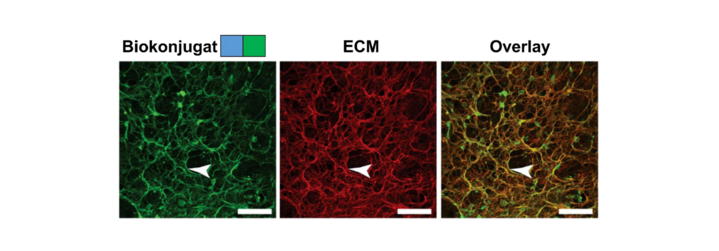
Abbildung 2: Mikroskopische Aufnahme der Fibronektin-gefärbten ECM (rot) mit verankertem Biokonjugat (grün)
Welche Ziele verfolgt das Projekt?
Das Hauptziel ist, die Wirksamkeit der Immuntherapie zu verbessern.
Konkret soll:
- ein neuer Wirkstoff entwickelt werden, der gezielt im Tumor wirkt
- verstanden werden, wie dieser Wirkstoff im Tumorgewebe verteilt wird
- getestet werden, ob sich dadurch die Reaktion auf Immuntherapien verbessert
- die Methode in patientennahen Modellen überprüft werden.
Langfristig geht es darum, Patientinnen und Patienten, die bisher nicht auf eine Immuntherapie ansprechen, neue Behandlungsmöglichkeiten zu eröffnen.
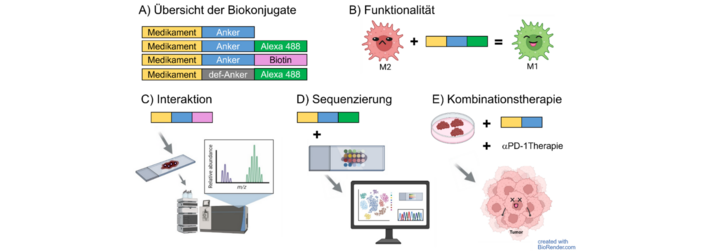
Abbildung 3: Grafische Übersicht des Projekts. A) Schematische Darstellung der im Projekt hergestellten Biokonjugate (def-Anker = defekter Anker, Kontrolle). B) Analyse der funktionellen Effekte der Biokonjugate auf die Polarisierung von Makrophagen. C) Massenspektrometrische Identifikation von ECM-Komponenten im Tumor, die von den Biokonjugaten gebunden werden. D) Räumliche Transkriptomanalyse (SpatialSeq) von Patientengewebe zur Untersuchung der Interaktionen zwischen ECM-produzierenden Zellen und TAMs sowie deren Einfluss auf das Tumormilieu. E) Anwendung der Biokonjugate auf frischem Tumorgewebe in Kombination mit einer Immuntherapie
Ansatz des Forschungsprojektes
Der Ansatz lässt sich vereinfacht so erklären:
Ein bekanntes Medikament wird zu einem Biokonjugat verändert, sodass es sich gezielt in der extrazellulären Matrix (ECM) des Tumors „verankern“ lässt (siehe Abbildung 2). Die ECM ist dabei das „Stützgerüst“ außerhalb der Zellen, welches Stabilität und Wachstum des Gewebes steuert und in Tumoren auch den Zugang für Immunzellen und Medikamente beeinflusst.
Aktiviert wird das Biokonjugat erst durch spezifische Enzyme aus dem Tumorumfeld. Nach der Freisetzung bewirkt das Medikament, dass TAMs wieder eine tumorbekämpfende statt einer tumorfördernden Funktion einnehmen.
In Kollaboration mit der AG Meinel (Lehrstuhl für Pharmazeutische Technologie und Biopharmazie, Julius-Maximilians-Universität Würzburg) kommen verschiedene Methoden zum Einsatz (Abbildung 3).
Neben der Synthese und Charakterisierung der Biokonjugate wird untersucht, wie diese die Polarisierung der Makrophagen in tumorbekämpfende bzw. tumorfördernde Zustände beeinflussen. Hierfür werden unter anderem Durchflusszytometrie, qRT-PCR und ELISA zur Analyse von Oberflächenmarkern und Zytokinprofilen eingesetzt. Funktionelle Effekte werden mittels T-Zell-Aktivierungs- und Phagozytose-Assays evaluiert.
Darüber hinaus wird die patientenspezifische ECM hinsichtlich ihrer Zusammensetzung charakterisiert: Tumorgewebe wird mit den Biokonjugaten inkubiert, und gebundene ECM-Komponenten werden mittels Massenspektrometrie identifiziert. Ergänzend wird mithilfe moderner räumlich aufgelöster Sequenzierverfahren (Spatial Sequencing) analysiert, welche ECM-produzierenden Zellpopulationen die TAMs beeinflussen und wie sich dies auf das Tumormikromilieu auswirkt. Schließlich wird an frischem Tumorgewebe untersucht, ob die Biokonjugate das Ansprechen auf Immuntherapien verbessern können.
Ziel ist die Entwicklung einer präzisen und zielgerichteten Krebstherapie, die direkt im Tumormikromilieu wirkt und bislang therapieresistente Patientinnen und Patienten besser erreicht.
Welche Krebserkrankung soll behandelt werden?
Das Projekt konzentriert sich auf das metastasierte Melanom, eine aggressive Form von Hautkrebs. Jedoch erhoffen wir uns durch die Charakterisierung der ECM-Komponenten die Anwendbarkeit dieser Biokonjugate auf andere Krebserkrankungen auszuweiten. Auch in anderen Tumorarten wie z.B. Brust-, Bauspeicheldrüsen- oder Darmkrebs spielt das TAM-vermittelte immunsuppressive TME eine große Rolle bei dem Ansprechen auf Therapien.
Warum soll das Forschungsprojekt unterstützt werden?
- Hoher Bedarf - Viele Betroffene haben derzeit keine wirksame Therapieoption.
- Neuer Ansatz - Es wird ein grundlegend neuer Weg verfolgt, nicht nur bestehende Therapien optimiert.
- Gezielte Wirkung - Der Wirkstoff entfaltet seine Wirkung direkt im Tumor und kann Nebenwirkungen verringern.
- Breite Anwendbarkeit - Der Ansatz könnte später auch bei anderen Krebsarten eingesetzt werden.
- Praxisnähe - Tests an patientennahen Modellen machen eine spätere Anwendung realistisch.
Insgesamt hat das Projekt das Potenzial, die Krebsbehandlung nachhaltig zu verbessern und mehr Patientinnen und Patienten zu helfen.
- Nächstes
- Forschungsprojekte
- Vorheriges
