Die Rolle des oralen Mikrobioms bei der Immuntherapie von Kopf-Hals-Tumoren

Abbildung 1: Interdisziplinäres Team mit Expertise in Kopf-Hals-Onkologie, Parodontologie und translationaler Forschung. Dr. Marius Hörner, MSc; PD Dr. Dr. Andreas Vollmer; Prof. Dr. Yvonne Jockel-Schneider, MSc; Prof. Dr. Dr. Stefan Hartmann (von links nach rechts).
TEAM
Unser junges und interdisziplinäres Team vereint Expertise aus der klinischen Kopf-Hals-Chirurgie, der Parodontologie und geriatrischen Zahnmedizin sowie der immunologischen und mikrobiologischen Diagnostik.
Im Mittelpunkt steht die Frage, wie das orale Mikrobiom und chronische entzündliche Prozesse, wie sie bei Parodontitis auftreten, das Ansprechen auf Immuntherapien bei Kopf-Hals-Tumoren beeinflussen und wie sich diese Faktoren unter laufender Immuntherapie dynamisch verändern. Ziel ist es, frühzeitig Hinweise auf ein Therapieansprechen zu identifizieren und so Behandlungen patientenzentrierter, schonender und wirksamer zu gestalten.
Motivation und Innovation
Die Immuntherapie hat die Behandlung von Kopf-Hals-Tumoren grundlegend erweitert. Dennoch profitieren nicht alle Patientinnen und Patienten gleichermaßen davon. Die Ursachen für dieses unterschiedliche Therapieansprechen sind bislang unzureichend verstanden. Ein innovativer Ansatz unserer Arbeitsgruppe ist die Untersuchung des oralen und intratumoralen Mikrobioms. Aktuelle Forschung zeigt, dass mikrobielle Gemeinschaften das Immunsystem modulieren und eine zentrale Rolle für Tumorprogression und Therapieansprechen spielen können. Insbesondere beeinflussen orale Pathobionten immunologische Signalwege, die für die Wirksamkeit von Immuncheckpoint-Inhibitoren entscheidend sind. Chronische parodontale Entzündungen tragen über die Aktivierung systemischer Immunantworten, die Freisetzung proinflammatorischer Zytokine sowie die Modulation tumorassoziierter Immunzellen zur Entstehung eines tumorsupportiven Mikromilieus bei. Durch die Verknüpfung mikrobiologischer Analysen mit klinischparodontologischen Parametern entsteht ein translationaler Ansatz, der molekulare Mechanismen mit der klinischen Realität verbindet und neue Perspektiven für personalisierte Therapien eröffnet.
Wir prüfen die Hypothese, dass spezifische mikrobielle Signaturen und parodontale Entzündungsprozesse das Ansprechen auf neoadjuvante Immuntherapien bei Kopf-Hals-Plattenepithelkarzinomen vorhersagen und funktionell modulieren.
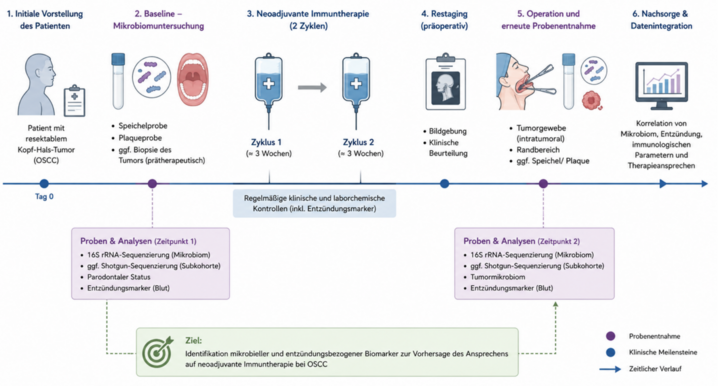
Abbildung 2: Schematische Darstellung des Studienablaufs
Gezeigt ist der zeitliche Ablauf des Projekts von der initialen Patientenvorstellung über die Baseline-Mikrobiomuntersuchung (Speichel, Plaque und Biopsie), zwei Zyklen neoadjuvanter Immuntherapie bis hin zur operativen Tumorresektion mit erneuter Probenentnahme. Während des gesamten Verlaufs erfolgen klinische und laborchemische Kontrollen. Ziel ist die longitudinale Analyse des oralen und intratumoralen Mikrobioms sowie die Korrelation mit Entzündungsparametern und dem Therapieansprechen.
Welche Ziele verfolgt das Projekt?
Übergeordnetes Ziel des Projekts ist es, den Einfluss des oralen und intratumoralen Mikrobioms sowie der parodontalen Entzündung auf das Ansprechen einer neoadjuvanten Immuntherapie bei Kopf-Hals-Tumoren zu untersuchen.
- Mikrobielle Dynamik: Charakterisierung der Veränderungen des oralen und intratumoralen Mikrobioms während der Immuntherapie.
- Mikrobiom, Entzündung und Therapieansprechen: Analyse des Zusammenhangs zwischen mikrobiellen Profilen, parodontalem Entzündungsstatus und klinisch verfügbaren immunologischen Parametern (z. B. systemische Entzündungsmarker) sowie dem Therapieansprechen, um mikrobiell vermittelte immunologische Mechanismen zu identifizieren.
- Prädiktive Marker: Identifikation mikrobieller und entzündungsbezogener Biomarker zur frühen Vorhersage des Therapieerfolgs.
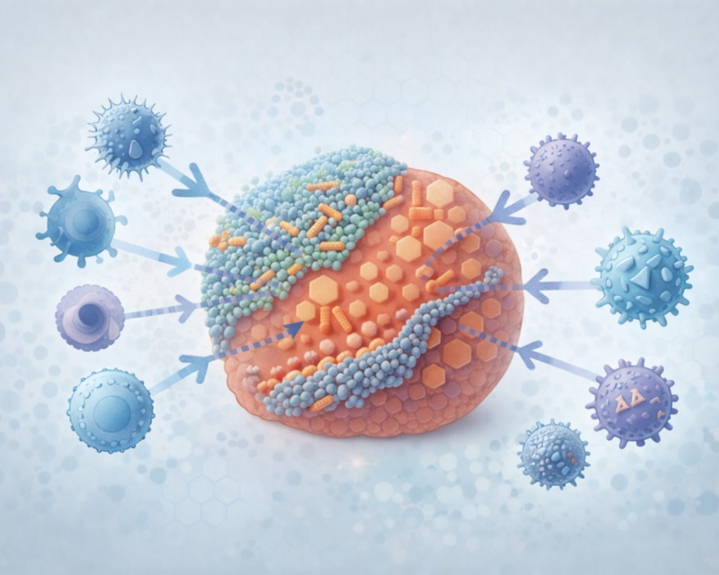
Abbildung 3: Interaktion Tumor und Mikrobiom
Schematische Darstellung der Interaktion zwischen Tumor, intratumoralem Mikrobiom und Immunantwort. Der Tumor ist zentral dargestellt und teilweise von organisierten biofilm-artigen mikrobiellen Gemeinschaften bedeckt bzw. durchsetzt. Diese mikrobiellen Aggregate repräsentieren eine strukturierte bakterielle Besiedlung des Tumorgewebes. Pfeile verdeutlichen schematisch eine Modulation tumoraler Signal- und Rezeptorzonen in räumlicher Nähe zur mikrobiellen Besiedlung. Umgebende abstrahierte Immunzellen zeigen eine abgeschwächte Signalübertragung zum Tumor, was mögliche indirekte Effekte der mikrobiellen Tumorbesiedlung auf die Immuninteraktion symbolisiert. Die Darstellung ist konzeptionell vereinfacht und dient der Illustration potenzieller biologischer Zusammenhänge, ohne spezifische Bakterienarten, Signalwege oder therapeutische Effekte abzubilden.
Ansatz des Forschungsprojektes
Patientinnen und Patienten mit einem operabel behandelbaren Kopf-Hals-Tumor erhalten vor der geplanten Operation eine Immuntherapie über einen Zeitraum von etwa sechs Wochen. Dieses Zeitfenster stellt ein klinisch relevantes „Beobachtungsfenster“ dar.
Im Rahmen der Studie werden Speichel- und Plaqueproben aus der Mundhöhle sowie Tumorgewebe mikrobiologisch untersucht. Ergänzend erfolgt eine standardisierte klinischparodontologische Untersuchung (u. a. Bleeding on Probing, parodontaler Status), um den oralen Entzündungsgrad differenziert zu erfassen.
Parodontitis dient hierbei als klinisch etabliertes und standardisiert messbares Modell chronischer Entzündung und ermöglicht eine einzigartige Verknüpfung zwischen lokaler mikrobieller Dysbiose und systemischer Immunmodulation. Ergänzend werden klinischverfügbare immunologische Parameter (z. B. systemische Entzündungsmarker und Routinelaborparameter) erfasst.
Die mikrobiologische Analyse erfolgt mittels eines kombinierten Ansatzes aus 16S-rRNASequenzierung zur breiten Charakterisierung des Mikrobioms sowie ergänzender ShotgunSequenzierung in einer definierten Subkohorte. Dadurch können neben der taxonomischen Zusammensetzung auch funktionelle mikrobielle Eigenschaften, Virulenzfaktoren und immunologisch relevante Signalwege erfasst werden, die mit dem Therapieansprechen assoziiert sind. Diese Analysen sollen insbesondere funktionelle Zusammenhänge zwischen mikrobiellen Profilen und dem individuellen Therapieansprechen auf Immuncheckpoint-Inhibitoren aufzeigen.
Welche Krebserkrankung soll behandelt werden?
Untersucht wird das orale Plattenepithelkarzinom (OSCC), eine häufige und oft aggressive Tumorerkrankung der Mundhöhle und angrenzender Strukturen. Diese Tumorentität ist klinisch von hoher Relevanz, da sie häufig erst in fortgeschrittenen Stadien diagnostiziert wird und mit einer erheblichen Beeinträchtigung von Funktion und Lebensqualität einhergeht.
Warum soll das Forschungsprojekt unterstützt werden?
Das Projekt stellt eine der ersten prospektiven Studien dar, die das orale und intratumorale Mikrobiom im Kontext einer neoadjuvanten Immuntherapie beim OSCC longitudinal untersucht. Es verbindet moderne Immunonkologie mit einem innovativen biologischen Ansatz und ist direkt aus der klinischen Versorgung heraus entstanden. Damit adressiert es eine zentrale Herausforderung der Onkologie: die Vorhersage des individuellen Therapieansprechens. Durch die systematische Integration mikrobieller Profile und parodontaler Entzündungsprozesse eröffnet das Projekt neue Perspektiven zur Erklärung interindividueller Therapieunterschiede und legt die Grundlage für personalisierte Behandlungsstrategien.
- Nächstes
- Forschungsprojekte
- Vorheriges
