Cholesterinstoffwechsel als therapeutischer Mechanismus gegen frühe Brustkrebsmetastasierung

Abbildung 1: Forschungsteam des Teilprojekts zur Rolle des Cholesterinstoffwechsels in der Brustkrebsmetastasierung (AG Riedel). Von links: Dr. Angela Riedel (Arbeitsgruppenleiterin), Finja Preikschardt (Masterandin) und Maximilian Krämer (Doktorand).
TEAM
Das junge Forschungsteam von Dr. Angela Riedel am Mildred-Scheel-Nachwuchszentrum für Krebsforschung (UKW) befasst sich mit der zellulären Kommunikation von Brustkrebszellen mit ihrer Umgebung und welchen Einfluss diese Kommunikation auf Prozesse wie Metastasierung und den intrazellulären Stoffwechsel hat.
Motivation und Innovation
Brustkrebs gehört weltweit zu den häufigsten Krebserkrankungen bei Frauen und ist weiterhin eine der häufigsten krebsbedingten Todesursachen. Besonders entscheidend für den Krankheitsverlauf ist die Metastasierung, also die Ausbreitung von Tumorzellen in andere Organe, die häufig mit einer Verschlechterung der Prognose und Therapieresistenz einhergeht.
Das internationale Forschungsteam der Arbeitsgruppe Riedel untersucht diese Prozesse mit besonderem Fokus auf den Lymphknoten als zentrale Schnittstelle zwischen Tumor und Immunsystem.
Im Zentrum unserer Arbeit steht die Frage, wie Tumorzellen diese eigentlich schützende Immunumgebung verändern und so Bedingungen schaffen, die ihr eigenes Wachstum unterstützen. Dabei richten wir den Blick besonders auf Stoffwechselprozesse, da diese sowohl die Funktion von Immunzellen als auch das Verhalten von Tumorzellen im Lymphknoten beeinflussen.
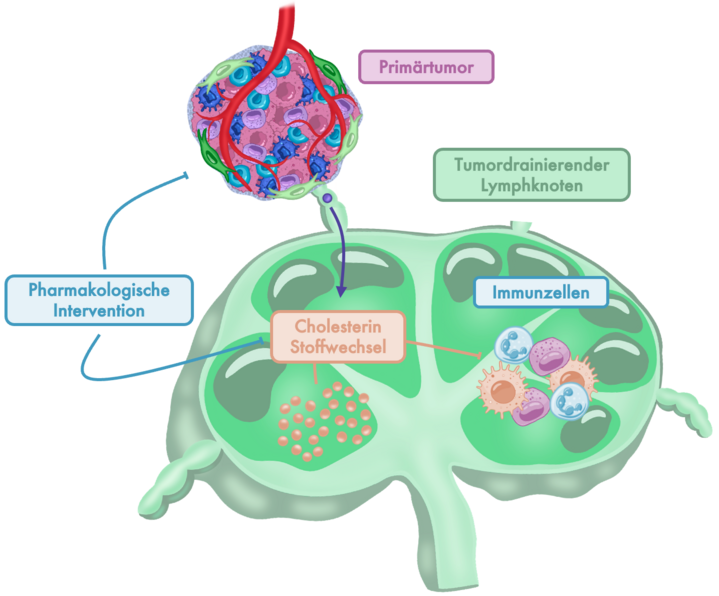
Abbildung 2: Schematische Darstellung des vorgestellten Mechanismus. Während der Tumorprogression verändert der Primärtumor den Cholesterinstoffwechsel im tumordrainierenden Lymphknoten. Dies führt zu einer eingeschränkten Funktion der Immunzellen und begünstigt die Ausbildung einer metastasenfördernden Mikroumgebung. Eine Intervention mit Statinen wirkt dabei potenziell zweifach: direkt auf den Primärtumor und zusätzlich über die Modulation des Cholesterinstoffwechsels auf die Wiederherstellung der Immunfunktion im Lymphknoten.
Welche Ziele verfolgt das Projekt?
Ziel des Projekts ist es, die Rolle des Cholesterinstoffwechsels bei frühen Veränderungen der Tumor-Mikroumgebung im Lymphknoten beim triple-negativen Brustkrebs besser zu verstehen. Auf dieser Grundlage sollen neue Ansatzpunkte identifiziert werden, um die cholesterinabhängige Umprogrammierung der Lymphknoten-Mikroumgebung gezielt zu beeinflussen und die frühe Metastasierung zu verhindern.
Bei Patientinnen mit frühem triple-negativem Brustkrebs spricht die Erkrankung häufig zunächst gut auf eine neoadjuvante Chemotherapie, teilweise auch in Kombination mit Immuntherapien, an. Dennoch entwickeln 30-40 % der Patientinnen innerhalb von fünf Jahren Metastasen, die oft auch im Lymphknoten sichtbar werden.
Dabei zeigt sich ein grundlegendes Paradox: Der Lymphknoten ist eigentlich ein zentrales Organ der Immunabwehr und sollte Tumorzellen erkennen und bekämpfen. Trotzdem kann er sich im Verlauf der Erkrankung zu einer Station der Tumorausbreitung entwickeln. Wir gehen davon aus, dass Tumorzellen diese Veränderung aktiv beeinflussen. Unsere bisherigen Arbeiten deuten darauf hin, dass dabei insbesondere der Cholesterinstoffwechsel eine wichtige Rolle spielt. Er wird durch das Zusammenspiel von Tumorzellen und Immunzellen verändert und beeinflusst sowohl die Funktion von Immunzellen als auch das Verhalten der Tumorzellen selbst.
Ziel ist es, diese Veränderungen im Cholesterinstoffwechsel systematisch zu untersuchen und besser zu verstehen, wie sie zur frühen Metastasierung beitragen. Darauf aufbauend sollen gezielt bereits zugelassene Medikamente eingesetzt werden, die den Cholesterinstoffwechsel modulieren. Dadurch soll geprüft werden, ob sich diese Prozesse beeinflussen lassen und sich die Immunfunktion im Lymphknoten wieder herstellen lässt.
Ansatz des Forschungsprojektes
Im Rahmen des Projekts analysieren wir Lymphknotengewebe sowie Lymphflüssigkeit aus dem tumordrainierenden Lymphknoten von Patientinnen mit triple-negativem Brustkrebs im frühen Stadium nach neoadjuvanter Therapie. Diese Proben ermöglichen einen direkten Einblick in frühe Veränderungen der Tumor-Mikroumgebung unter klinisch realen Bedingungen.
Unser Fokus liegt dabei auf dem Cholesterinstoffwechsel als zentralem metabolischen Knotenpunkt. Dieser kann beispielsweise durch Statine moduliert werden, eine klinisch etablierte Wirkstoffklasse zur Behandlung von Herzinfarkt- und Schlaganfallpatienten. Es wurde in Studien gezeigt, dass durch die Gabe von Statinen, insbesondere in Kombination mit Immuntherapien, ein schützender Effekt auf das Auftreten eines Rezidivs bei Brustkrebspatientinnen erzielt werden kann. Der genaue Wirkmechanismus von Statinen, insbesondere in Bezug auf die Bildung von Metastasen in Lymphknoten und anderen Organen bei Brustkrebs, ist bisher aber unzureichend verstanden. Wir möchten daher untersuchen, welche Auswirkungen die Gabe von Statinen auf die Funktion der Immunzellen im Lymphknoten hat und ob dadurch frühe tumorassoziierte Veränderungen der Mikroumgebung abgeschwächt werden können.
Zur Analyse dieses Mechanismus setzen wir lipidomische Verfahren ein, um cholesterinbezogene Veränderungen in der Lymphknoten-Mikroumgebung präzise zu erfassen. Ergänzend entwickeln wir funktionelle Modelle, in denen diese Veränderungen nachgebildet und gezielt getestet werden können. Dabei prüfen wir, ob sich sowohl die Tumorzellaktivität als auch die immunologische Dysfunktion im Lymphknoten gleichzeitig positiv beeinflussen lassen und sich die tumorassoziierte Umprogrammierung der Mikroumgebung, durch Nutzung von Cholesterinregulatoren, abschwächen lässt.
Damit eröffnet sich ein möglicher doppelter therapeutischer Ansatz: Statine könnten einerseits direkt auf den Primärtumor wirken, andererseits aber gleichzeitig die metabolische und immunologische Situation im Lymphknoten beeinflussen. Auf diese Weise wäre eine gezielte, über den Cholesterinstoffwechsel vermittelte Therapie an zwei funktionell verbundenen Orten der Tumorprogression möglich.
Welche Krebserkrankung soll behandelt werden?
Der Fokus liegt auf dem triple-negativen Brustkrebs, einer biologisch aggressiven Subform mit erhöhter Neigung zu früher Metastasierung und Krankheitsrückfällen. Für diese Tumorentität stehen bislang keine etablierten zielgerichteten Therapieoptionen zur Verfügung, sodass ein hoher Bedarf an neuen, mechanistisch basierten Behandlungsstrategien besteht.
Warum soll das Forschungsprojekt unterstützt werden?
Das Projekt adressiert eine bislang unzureichend genutzte therapeutische Möglichkeit in der frühen Metastasierung: die metabolische Umprogrammierung der Lymphknoten-Mikroumgebung. Während der Einfluss des Cholesterinstoffwechsels und von Statinen auf den Primärtumor bereits untersucht wurde, ist ihre Rolle im tumordrainierenden Lymphknoten bislang kaum verstanden. Gerade dieser stellt jedoch einen zentralen Ort der frühen Tumorausbreitung dar.
Hier setzt das Projekt an und untersucht gezielt, wie cholesterinabhängige Prozesse die Immunzellfunktion im Lymphknoten beeinflussen und zur Ausbildung metastatischer Nischen beitragen. Durch die Kombination aus patientennaher Probenanalyse, funktionellen Modellen und gezielten pharmakologischen Interventionen werden diese metabolischen Veränderungen systematisch untersucht und in ihrer funktionellen und therapeutischen Relevanz bewertet.
Damit verfolgt das Projekt einen klar translationalen Ansatz, der über rein beschreibende Analysen hinausgeht und neue Perspektiven für die Verhinderung früher Metastasierung bei aggressiven Tumorerkrankungen eröffnen kann.
- Nächstes
- Forschungsprojekte
- Vorheriges
