Aspergillus-CMV-Koinfektion nach alloSZT im humanen 3D-Lungenmodell

Abbildung 1: Das Team der AG Löffler (links) und Dr. Chris Lauruschkat (rechts)
Das Team arbeitet seit über 20 Jahren in der Diagnostik und Forschung von Pilzinfektionen mit speziellem Fokus auf invasive Aspergillosen. Neben dem Arbeitsgruppenleiter, Prof. Dr. Jürgen Löffler, gehören dem Team momentan drei Postdoktoranden, zwei biologische Doktorandinnen und mehrere medizinisch-technische Assistentinnen an. Dr. Chris Lauruschkat ist ehemaliger Doktorand der AG Löffler und mittlerweile als Postdoc und Projektleiter in der AG Kraus tätig. Sein Forschungsschwerpunkt sind Infektionen nach allogener Stammzelltransplantation mit Fokus auf Zytomegalievirus (CMV) und dem adaptiven Immunsystem.
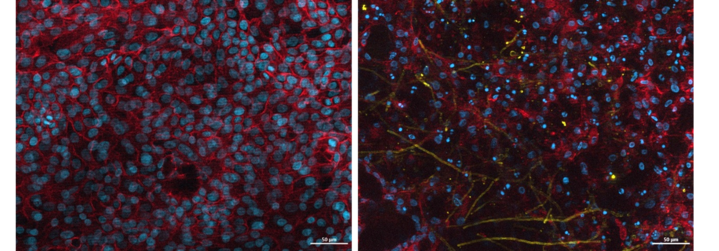
Abbildung 2: Fluoreszenzmikroskopische Darstellung einer uninfizierten (links) und einer mit Aspergillus fumigatus infizierten Einzelzellschicht (rechts), die aus Lungenorganoiden hergestellt wurden. Der Pilz zerstört die Epithelzellschicht und führt in Folge zum Zelltod, charakterisiert durch die Fragmentierung der Zellkerne
Motivation und Innovation
Nach einer allogenen Stammzelltransplantation (alloSZT) sowie bei neueren Immuntherapien gegen Krebs ist das Immunsystem der Patienten oft stark und über längere Zeit geschwächt. Grund hierfür sind die Grunderkrankung und die daraus resultierenden intensiven Behandlungen. Dadurch steigt das Risiko für sogenannte opportunistische Infektionen, also Infektionen mit Erregern, die vor allem bei einem geschwächtem Immunsystem gefährlich werden können, deutlich an.
Bei Patienten nach alloSZT ist CMV der relevanteste virale Erreger, während Aspergillus, ein Schimmelpilz, der wichtigste Pilzerreger ist. Beide Infektionen können schwere Krankheitsverläufe verursachen und die Sterblichkeit dieser Patienten deutlich erhöhen. Besonders wichtig und gefährlich für Patienten ist das Zusammenspiel zwischen Virus- und Pilzinfektionen. Eine CMV-Infektion kann die Immunabwehr gegen Pilze aktiv schwächen. Dadurch steigt das Risiko, dass Patienten gleichzeitig an der CMV-Infektion und an einer Aspergillus-Infektion erkranken; eine sogenannte Koinfektion. Solche Koinfektionen mit CMV und Aspergillus sind mit einer sehr hohen Sterblichkeit verbunden. Entscheidend für die Schwere des Krankheitsverlaufs ist wahrscheinlich das Zusammenspiel verschiedener Immunzellpopulationen mit den beiden Erregern. Dazu gehören Zellen der angeborenen und der adaptiven Immunantwort.
Klassische Zellkulturen und Tiermodelle können die menschliche Lunge nur begrenzt nachbilden. 3D-Lungenorganoide bieten daher ein neues innovatives Modell, um Interaktionen von Erregern und Immunzellen in der Lunge zu untersuchen.
Welche Ziele verfolgt das Projekt?
Ziel des Projekts ist es, neuartige 3D-Lungenorganoide einzusetzen, um die Koinfektion von CMV und Aspergillus und deren Interaktion mit verschiedenen Immunzellen bei immungeschwächten Krebspatienten zu erforschen. So sollen bisher unbekannte Mechanismen der Immunabwehr aufgedeckt und langfristig neue Ansätze für Vorbeugung, Diagnose und Behandlung ermöglicht werden.
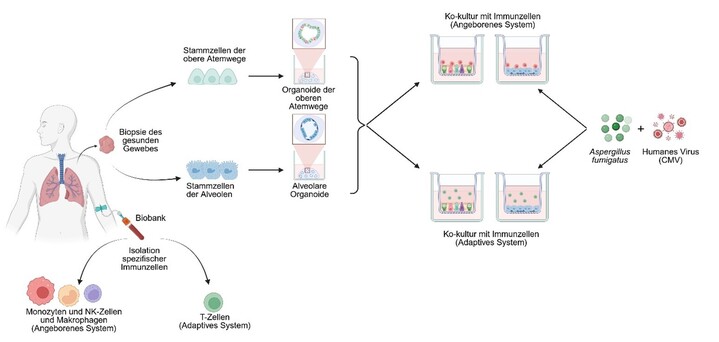
Abbildung 3: Schematische Darstellung der Arbeitsschritte unseres Projektes
Ansatz des Forschungsprojektes
Der zentrale Ansatz des Projekts besteht darin, aus humanem Lungengewebe so genannte 3D-Lungenorganoide im Labor herzustellen. Das humane 3D-Lungenorganoidmodell bildet zentrale strukturelle und funktionelle Eigenschaften des menschlichen Lungengewebes realitätsnah nach. Dieses Modell wird mit autologen, also patienteneigenen Immunzellen kombiniert. Dies ist von Bedeutung, da autologe Immunzellen die individuelle Patientensituation besser widerspiegeln als Fremdzellen und zugleich unerwünschte Reaktionen bestimmter Immunzellpopulationen gegen fremdes Gewebe verhindern können. Das System wird eingesetzt, um CMV- und Aspergillus-Einzelinfektionen mit einer Koinfektion zu vergleichen und deren jeweilige Interaktionen mit dem humanen Immunsystem zu untersuchen.
Unsere Arbeitsgruppe konnte, mit Unterstützung unseres Kooperationspartners am Robert-Koch-Institut in Berlin (PD Dr. Volker Rickerts), diese komplexen 3D-Lungenorganoidmodell vor Ort erlernen, und sie momentan an das UKW transferieren und im hiesigen Labor etablieren.
Welche Krebserkrankung soll behandelt werden?
Unser Projekt liefert Erkenntnisse, die für viele stark immungeschwächte Patienten wichtig sind. Besonders betrifft dies Menschen nach einer alloSZT oder mit akuten Leukämien. Auch andere Patientengruppen haben ein erhöhtes Risiko für solche Infektionen. Dazu gehören zum Beispiel Menschen, die bestimmte Immuntherapien erhalten, bei denen Immunzellen über längere Zeit stark vermindert sind, wie beispielsweise Patienten, die mit sogenannten BTK Hemmern wie Ibrutinib behandelt werden.
Warum soll das Forschungsprojekt unterstützt werden?
Infektionen mit CMV und Aspergillus stellen gefährliche Komplikationen bei Krebspatienten dar, insbesondere nach alloSZT. Bislang sind sie schwer zu diagnostizieren und zu behandeln. Besonders kritisch ist es, wenn beide Infektionen gleichzeitig auftreten, da der Verlauf dann meist schwerwiegender ist und zu einer deutlich höheren Sterblichkeit führt. Das Projekt soll daher helfen, zu verstehen, warum diese Infektionen entstehen und weshalb sie bei manchen Krebspatienten sehr schwer verlaufen. Langfristig können dadurch Hochrisikopatienten gezielter behandelt, schwere Verläufe verhindert, Überlebenschancen verbessert und unnötige oder belastende Therapien reduziert werden.
Perspektivisch kann das entwickelte 3D-Lungenorganoidmodell mit autologen Immunzellen auch genutzt werden, um weitere wichtige Lungeninfektionen bei Krebspatienten zu erforschen. Das Modell ist besonders wertvoll, da Gewebeproben aus der Lunge bei solchen Infektionen meist sehr schwer zu entnehmen sind.
- Nächstes
- Forschungsprojekte
- Vorheriges
