Präklinische Charakterisierung von CAR-T assoziierten Leukämien bei Patienten mit Multiplem Myelom
Dieses Projekt wurde 2024 von der Stiftung "Forschung hilft" mit 15.000 Euro gefördert.

Abbildung 1: Gruppenfoto der AG Waldschmidt
Team
Unsere Arbeitsgruppe setzt sich zusammen aus jungen Wissenschaftlerinnen und Wissenschaftlern mit ausgewiesener Expertise in den Bereichen der Molekulargenetik und Bioinformatik. Die Projektdurchführung erfolgt in enger Abstimmung mit den Arbeitsgruppen von Prof. Rasche und Prof. Kortüm sowie Kooperationspartnern am Universitätsklinikum Helsinki (Finnland) und an der Harvard Medical School in Boston (USA).
Motivation und Innovation
Die Prognose von Patientinnen und Patienten mit Krebserkrankungen hat sich in letzten Jahren durch den Einsatz zellulärer Immuntherapien signifikant verbessert. Trotz ihrer beachtlichen Wirksamkeit bleibt insbesondere die Therapie mit chimären Antigen-Rezeptor-T (CAR-T)- Zellen ein junges Therapieverfahren, dessen Nebenwirkungen noch nicht vollumfänglich verstanden sind.
Unser Forschungsvorhaben soll dabei helfen, das Risiko von hämatologischen Zweitneoplasien nach CAR-T-Zelltherapie besser einschätzen zu können und leistet auf diese Weise einen wichtigen Beitrag zu einer noch sichereren Anwendung dieser hoch effektiven Therapieform.
Welche Ziele verfolgt das Projekt?
Kürzlich veröffentlichte Studiendaten zeigen für die Modellerkrankung Multiples Myelom ein relevant erhöhtes Risiko für das Auftreten therapie-assoziierter myeloischer Neoplasien nach Therapie mit dem anti-BCMA CAR-T-Zellprodukt Cilta-cel. Gleichzeitig wissen wir, dass auch andere Faktoren, wie beispielsweise das Alter oder eine langjährige Behandlung mit alkylierenden Chemotherapeutika die Entstehung von Zweittumoren bei Patienten mit Multiplem Myelom begünstigen können.
In diesem Vorhaben möchten wir daher die Hypothese untersuchen, ob eine vorbestehende klonale Hämatopoese von unbestimmtem Potential (clonal hematopoiesis of indeterminate potential, CHIP) im Knochenmark von Myelompatienten ein Risiko für die Entwicklung einer CAR-T assoziierten Sekundärleukämie darstellen könnte.
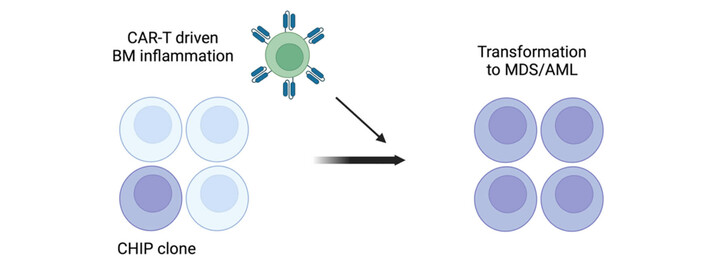
Abbildung 2: Knochenmark-vermittelte Inflammation und deren mögliche Auswirkung auf die Pathogenese von Sekundärleukämien (schematische Darstellung)
Ansatz des Forschungsprojektes
Wir postulieren, dass die CAR-T vermittelte Inflammation im Knochenmark einen relevanten Wachstumsstimulus für vorbestehende CHIP-Klone darstellt. Auf Basis korrelativer genetischer Daten aus drei unabhängigen klinischen Kohorten und unter Verwendung neuester CRISPR-Cas9-Technologie, werden wir ex vivo Ko-Kultur-Modelle entwickeln, die es uns erlauben die CAR-T vermittelte Inflammation im Knochenmark zu simulieren. Im ersten Schritt sollen TP53-Knockout-Modelle verschiedener Leukämie-Zelllinien etabliert werden. Unter Verwendung einer in unserem Labor entwickelten Ko-Kultur-Plattform (CoSeedis®) werden wir anschließend mittels klonalem Kompetitionsassay den Wachstumsvorteil von TP53-Knockouts unter inflammatorischen Ko-Kultur-Bedingungen analysieren. Um die Bedeutung unserer Beobachtung auch für andere CHIP-Mutationen abschätzen zu können, sollen im letzten Schritt dieses Projekts weitere primäre Zellkulturmodelle auf Basis von Mutationen in den CHIP-Genen TET2-, DNMT3A, PPM1D und ASXL1 generiert werden.
Welche Krebserkrankung soll behandelt werden?
Der Einfluss von CAR-T assoziierter Inflammation auf vorbestehende CHIP-Klone in der hämatopoetischen Nische wird am Beispiel der Modellerkrankung Multiples Myelom untersucht. Wir gehen davon aus, dass unsere Beobachtungen auch auf andere Krebserkrankungen, die mittels CAR-T-Zelltherapie behandelt werden, übertragbar sind.
Warum soll das Forschungsprojekt unterstützt werden?
Dieses Forschungsprojekt leistet einen wichtigen Beitrag zum besseren Verständnis von CAR-T assoziierten Sekundärleukämien bei Myelom-Patienten, mit unmittelbarer Relevanz für die sichere Anwendung von CAR-T-Therapien im klinischen Alltag.
