Das Gehirn vor Metastasen schützen
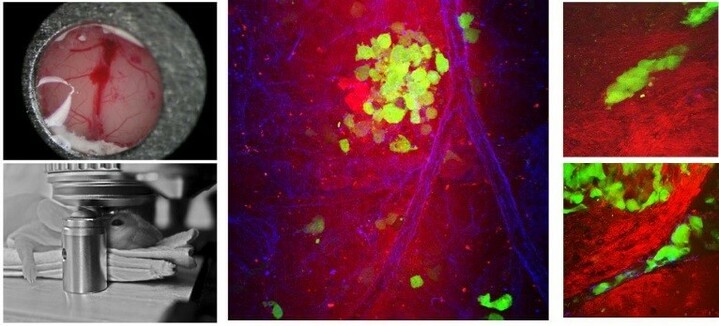
Abb 1: In vivo-Bildgebung von kortikalen Hirntumoren durch kraniale Fenster mittels markierungsfreier Multiphotonen-Bildgebung. Der Ort von Gliomzellen (GFP, grün) kann zwischen Blutgefäßen (blau) und Fasertrakten (rot) bestimmt werden.
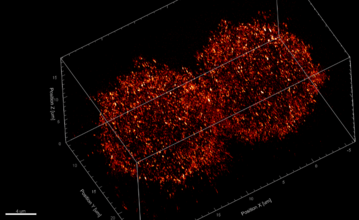
Abb 2: Hochauflösende dSTORM-Mikroskopie visualisiert die Verteilung von Membranrezeptoren (CD45) in der Plasmamembran einer von Jurkat-Zellen. (Wäldchen et al., Nat. Comm. DOI:10.1038/s41467-020-14731-0.)

Abb 3: Das interdisziplinäre Forscherteam von Prof. Dr. Carola Förster und Prof. Dr. Mario Löhr setzt sich aus erfahrenen Neuroonkologen, Biochemikern, Zell- und Molekularbiologen sowie technischen Assistenten zusammen.
Motivation und Innovation der Arbeitsgruppe
Die Motivation unserer AG: Entwicklung eines völlig neuartigen Therapieansatzes zur Prävention von Hirnmetastasen beim Brustkrebs durch Stärken der Barrierefunktion der Blut-Hirn-Schranke.
Beim Brustkrebs (Mammakarzinom) treten in bis zu 20% der Fällen Metastasen im Gehirn auf, die nicht nur zu einer deutlichen Einschränkung der Lebenserwartung der erkrankten Frauen führen, sondern auch mit neurologischen Ausfällen (bspw. Bewegungs-, Sprach- und Gedächtnisstörungen sowie epileptischen Anfällen) einhergehen und somit die Lebensqualität stark beeinträchtigen. Obwohl Hirnmetastasen in den meisten Fällen erst viele Monate bis mehrere Jahre nach der Erstdiagnose eines Mammakarzinoms Symptome verursachen, findet die Einwanderung der im Blut zirkulierenden Krebszellen in das Gehirn bereits in einem viel früheren Erkrankungsstadium statt, indem die Tumorzellen zunächst aus den Blutgefäßen austreten und die Blut-Hirn-Schranke durchdringen, die das empfindliche Hirngewebe vom Blutkreislauf abtrennt. Dies geschieht, indem sie sich an spezifische Oberflächenrezeptoren der Gefäßwandzellen binden und wie bei einer Entzündungsreaktion eine erhöhte Durchlässigkeit der Blut-Hirn-Schranke hervorrufen, was den metastasierenden Krebszellen das Durchdringen dieser Barriere und das Einwandern in das Gehirn ermöglicht. Bislang gab es keine Möglichkeit, die Invasion von metastasierenden Krebszellen ins Gehirn wirkungsvoll zu verhindern.
Mit einer völlig neuartigen endokrinen Kombinationstherapie soll die Blut-Hirn-Schranke gegen den Durchtritt von metastasierenden Brustkrebszellen abgedichtet werden. Die Ergebnisse unserer Versuche lassen sich später auch auf andere häufig in das Gehirn metastasierende Tumoren wie Lungenkrebs oder schwarzen Hautkrebs übertragen.
Projektziele
In ausführlichen Vorarbeiten haben wir entdeckt, dass die Barrierefunktion der Blut-Hirn-Schranke durch die Aktivierung bestimmter Östrogen-Rezeptor-Subtypen an den Gefäßwandzellen stabilisiert wird. Dieser Effekt wird durch die Anwendung entzündungshemmender und krebshemmender Naturstoffe sogar noch weiter verstärkt.
In unserem Forschungsprojekt sollen nun gezielt Stoffe, die an geeigneten Subtypen von Östrogenrezeptoren auf der Gefäßwand der Hirnzirkulation und auf den metastasierenden Brustkrebszellen andocken, zu einer neuartigen anti-metastatischen Therapie weiterentwickelt werden. Die hierdurch hervorgerufene Verstärkung der Blut-Hirn-Schranke soll ein Übertreten metastasierender Zellen aus dem Blutkreislauf in das Gehirn verhindern, wobei durch die Gabe entzündungshemmender Naturstoffe die Barriere-schwächende Entzündungsreaktion durch die Tumorzellen abgeschwächt wird und das Wachstum der metastasierenden Zellen zusätzlich durch krebshemmende Effekte der ausgewählten Naturstoffe eingedämmt wird. Durch eine Verabreichung der selektiven endokrinen Therapie in Form von Nanopartikeln und die verstärkende Anwendung entzündungs- und krebshemmender Naturstoffe sollen mögliche Nebenwirkungen eingeschränkt werden.
Ansatz des Forschungsprojektes
Unser Forscherteam möchte die Metastasierung von Brustkrebs in das Gehirn durch das Versiegeln der Blut-Hirn-Schranke mit einer Kombination aus einem zielgerichteten endokrinen Therapieansatz und entzündungshemmenden Naturstoffen verhindern. Metastasierende Krebszellen entwickeln verschiedene Strategien, die Durchlässigkeit der Blut-Hirn-Schranke zu erhöhen. Krebszellen können nämlich entzündliche Signalwege in den Gefäßzellen aktivieren, wodurch ihre Einwanderung in das Hirngewebe erleichtert wird. Wir haben die zugrundeliegenden molekularen Mechanismen bereits entschlüsselt und werden in diesem Forschungsprojekt erstmals analysieren, in welchem Ausmaß die Dichtigkeit der Blut-Hirn-Schranke durch die selektive Aktivierung bestimmter Östrogen-Rezeptor-Subtypen auf den Gefäßwandzellen gestärkt und somit der Durchtritt von Krebszellen verhindert werden kann. Die hierzu von uns entwickelte zielgerichtete endokrine Kombinationstherapie, deren Wirkung durch die gleichzeitige Gabe von entzündungshemmenden Naturstoffen verstärkt wird, soll zunächst an Zellkulturmodellen getestet und später in präklinischen Mausmodellen optimiert werden.
Krebserkrankung, die behandelt werden soll
Die Entstehung von Hirnmetastasen bei Brustkrebs soll verhindert werden. Die Ergebnisse unserer Untersuchungen lassen sich später auch auf andere häufig in das Gehirn metastasierende Tumoren wie Lungenkrebs oder schwarzen Hautkrebs übertragen.
Warum soll das Forschungsprojekt unterstützt werden?
Es handelt sich um den ersten zielgerichteten Ansatz, um das Auftreten von Hirnmetastasen bei Krebserkrankungen zu reduzieren. Falls sich diese neuartige Therapie als wirksam erweisen sollte, kann dadurch die Überlebenszeit und die Lebensqualität vieler an Brustkrebs erkrankter Frauen verbessert werden.
